Для перегляду доступних досліджень та термінів їх виконання

Сучасні можливості скринінгу хронічних гастритів. Фокус на атрофію
19.06.2023
Понад третина дорослого населення страждає на хронічний гастрит, проте до лікарів звертаються лише 10-15% таких хворих. Гастрит, спричинений H. pylori, переважає: його частота становить 80-90% усіх гастритів, частота аутоімунного гастриту — лише 10%. Реальна поширеність атрофії слизової оболонки шлунка невідома, але якщо розглядати її як прояв аутоімунного гастриту (АМАГ) і наслідок тривалого перебігу Хелікобактер пілорі - асоційованого гастриту, то частота атрофічного гастриту може сягати 50-60%.
Про сучасні можливості скринінгу хронічних гастритів: у фокусі на атрофію, розповіла під час свого виступу на ХХV Національній Школі гастроентерологів, гепатологів України «Актуальні діагностичні та терапевтичні досягнення в гастроентерології і гепатології», Губська Олена Юріївна, д.м.н., професор, завідувачка кафедри терапії, інфекційних хвороб та дерматовенерології Інституту післядипломної освіти НМУ імені О.О. Богомольця.
Хронічний гастрит, на сьогодні визначається, як хронічне запалення слизової оболонки шлунку з двома видами причин: інфекційний або аутоімунний.
Атрофічний гастрит (АГ) - це хронічне запалення, що супроводжується зміною клітин слизової оболонки шлунка за типом атрофії. Поділяється на види, що мають спільну гістологічну характеристику, а саме – Метаплазію слизової оболонки. Тому у назвах обох видів гастритів додано – метапластичний. Встановлені різні причини розвитку захворювання. Поява атрофічних змін у слизовій оболонці може бути наслідком патологічного процесу або вікових інволюційних змін, також можлива генетично обумовлена гіпо- або атрофія слизової оболонки шлунка. Найчастішими етіологічними факторами атрофічного гастриту визнано інфекцію Н. pylori й аутоімунний гастрит.
Аутоімунний метапластичний атрофічний гастрит -АМАГ – гастрит переважно тіла шлунка має основні характеристики:
- Поширеність 2%
- Асоційований з іншими аутоімунними станами
- + додаткові фактори, що необхідні до формування АМАГ – це вплив зовнішнього середовища – Hp-інфекція
- Виявлено зв’язок з певними генами: Гени - Gasa 1, 2, 3 на 4 та 6 хромосомах
- Визначається схильність до нейроендокринних пухлин шлунку та аденокарциноми
Мультифокальний АГ (ЕМАГ) Екзогенний метапластичний атрофічний гастрит – що асоційований з H. pylori, впливом факторів зовнішнього середовища, харчуванням.
У 1990 році в Сіднеї (Австралія) було прийнято нову класифікацію гастриту, що отримала назву Сіднейська система, згідно з якою діагноз гастриту має формулюватися на підставі:
- локалізації патологічного процесу;
- гістологічних ознаках, виявлених під час дослідження біоптатів;
- макроскопічних ознаках, виявлених під час ендоскопії;
- ймовірних етіологічних чинниках.
Пізніша Х’юстонська класифікація доповнила Сіднейську систему важливими чинниками, відповідно до яких розрізняють:
- хронічний гастрит неатрофічний (передусім спричинений H. pylori);
- хронічний атрофічний гастрит;
- мультифокальний гастрит (як результат тривалого перебігу гастриту, асоційованого з H. pylori);
- аутоімунний гастрит;
- особливі форми гастриту
Сьогодні Сіднейська система найчастіше застосовується, однак не має великого практичного значення щодо прогнозу раку шлунка у хворих з атрофічним гастритом.
Шляхи формування атрофічного гастриту:
- Безпосередня деструкція залозистого епітелію шлунка або його деструкція внаслідок хронічного запалення
- Виборча деструкція спеціалізованих епітеліоцитів в умовах збереження стовбурових клітин
Візитівкою природного плину хронічного атрофічного гастриту (ХАГ) є метаплазія – переважно інтестинальна.
Метаплазія вважається універсальною характеристикою і морфологічною особливістю ХАГ, та високорелевантна в патогенезі цього гастриту і його ускладнень: перніциозної анемії, дисплазії, раку шлунку. «Діагноз кишкової метаплазії на гістопатологічному дослідженні шлунка передбачає діагноз атрофічного гастриту, оскільки кишкова метаплазія відбувається в підлеглій атрофічній слизовій оболонці, хоча це часто чітко не зазначено в гістопатологічних звітах». (Оновлення клінічної практики AGA щодо діагностики та лікування атрофічного гастриту: експертний огляд)
У патогенезі прогресування від передракових станів до аденокарциноми шлунка кишкового типу, згідно із запропонованим каскадом Correa, вважають перехід від нормального епітелію шлунка через запалення, атрофію, внутрішньослизову карциному, і нарешті — до прогресування, інвазивної карциноми. «Атрофічний гастрит є важливою стадією з виразними гістопатологічними змінами в багатоступеневому каскаді патогенезу раку шлунка» (Оновлення клінічної практики AGA щодо діагностики та лікування атрофічного гастриту: експертний огляд)
Каскад передракових змін при атрофічному гастриті: атрофія - шлунково-кишкова метаплазія – дисплазія - аденокарцинома шлунка.

У 2008 році група експертів (M. Rugge, P. Correa, F. di Mario та ін.) запропонувала нову класифікацію ХГ – систему OLGA (Оperative Link for Gastritis Assessment), яка враховувала певні недоліки Сіднейсько-Х'юстонської класифікації. В OLGA застосовують оцінку гістологічних ознак вираження запалення й атрофії в антральному відділі та тілі шлунка з подальшим визначенням інтегральних показників – ступеня і стадії гастриту. Під ступенем гастриту розуміють ступінь вираження сумарної запальної інфільтрації, під стадією – ступінь вираження атрофії. Система OLGA порівняно з попередньою класифікацією дозволяє підвищити якість стратифікації ризику виникнення раку шлунку у пацієнта. Мається на увазі, що чим більший ступінь вираження атрофії та обсяг ураження, тим вищий ризик раку.
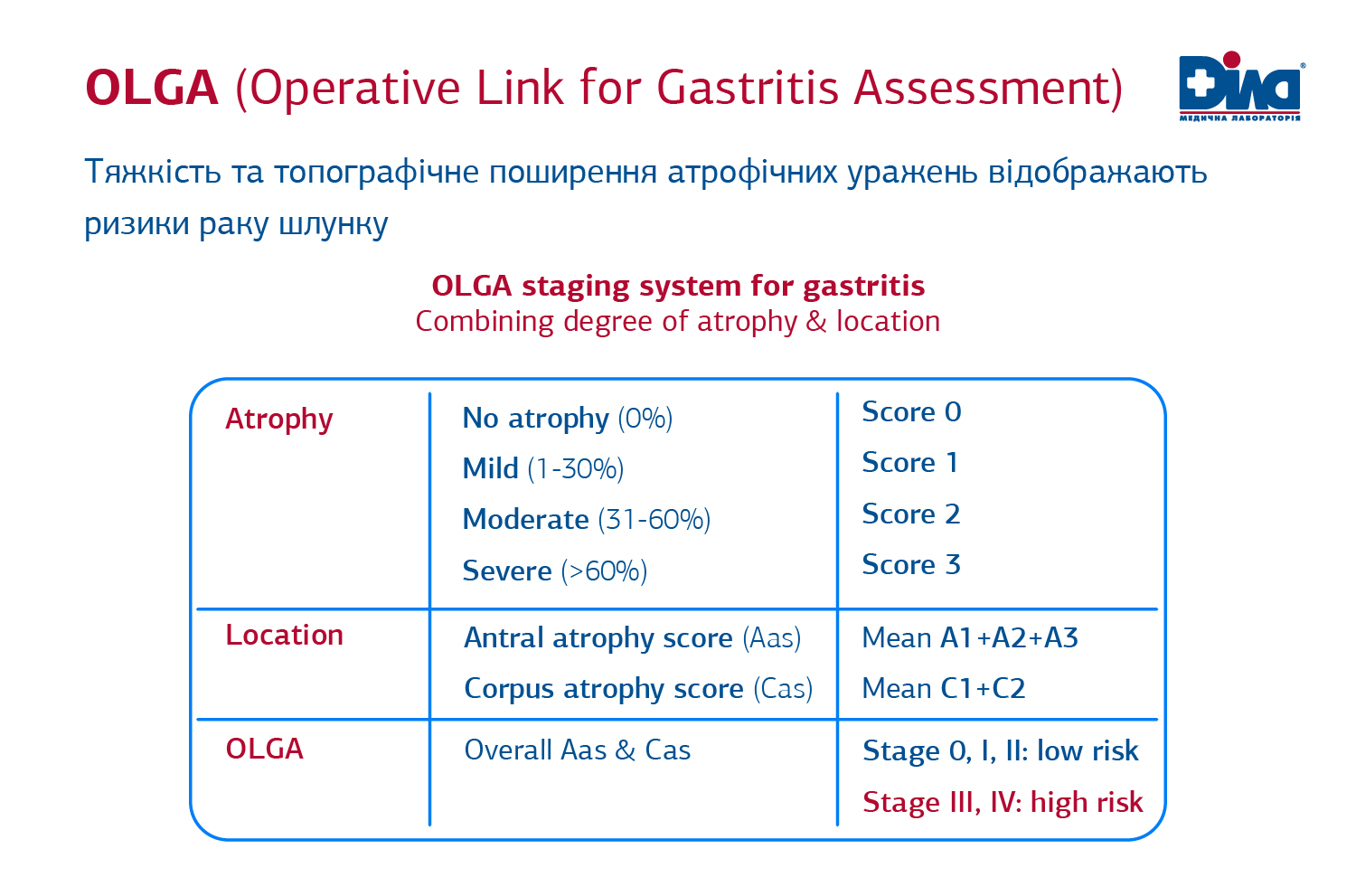
Встановлення діагнозу атрофічного гастриту дозволяє на ранніх стадіях виявити рак шлунку.
Більше інформації щодо ведення хворих з ХАГ, згідно з отриманими ендоскопічними даними, надають оновлені гайдлайни, а саме Guideline update 2019: Ведення епітеліальних передракових станів та уражень шлунка (MAPS II); Європейське товариство шлунково-кишкової ендоскопії (ESGE), Європейська дослідницька група з Helicobacter and Microbiota (EHMSG), Європейське товариство патології (ESP) і Sociedade Portuguesa de Endoscopia Digestiva (SPED) оновлення рекомендацій 2019:
Пацієнти з хронічним атрофічним гастритом або кишковою метаплазією (ІМ) знаходяться в групі ризику розвитку аденокарциноми шлунка.
- Для пацієнтів із легкою та помірною атрофією, обмеженою антральним відділом, немає доказів, які б рекомендували спостереження;
- У пацієнтів з кишковою метаплазією (IM) в одній локалізації, але з сімейним анамнезом раку шлунка, неповного розвитку (ІМ) або стійкого Helicobacter pylori гастриту, ендоскопічне спостереження з хромоендоскопією (CE) та керованими біопсіями можна розглянути через 3 роки;
- Пацієнти з пізніми стадіями атрофічного гастриту повинні проходити якісне ендоскопічне обстеження кожні 3 роки;
- У пацієнтів з дисплазією, за відсутності ендоскопічно визначеного ураження, рекомендується негайна високоякісна ендоскопічна оцінка з хромоендоскопією (CE);
- Пацієнти з ендоскопічно видимим ураженням, що містить дисплазію або карциному низького або високого ступеня, повинні пройти визначення стадії та лікування.
Біопсії слід брати принаймні з двох топографічних ділянок (антрум і корпус) і маркувати у двох окремих флаконах. Ерадикація H. pylori виліковує неатрофічний хронічний гастрит, може призвести до регресії атрофічного гастриту та знижує ризик раку шлунка у пацієнтів із цими станами, і це рекомендовано. Ерадикація H. pylori також рекомендована пацієнтам з неоплазією після ендоскопічної терапії.»

Важливим моментом сучасної діагностики ХАГ є можливість перемикання на неінвазивні підходи. Достатньо давно в арсеналі лікарів з’ явився Метод серологічної біопсії, а саме наявність унікальних високо специфічних аналізів крові, що дозволяють проводити скринінг атрофічного гастриту, раку шлунка, особливо в країнах з високою поширеністю цих захворювань.

Чому така назва?
Дослідженнями було підтверджено високу кореляцію серологічних маркерів: пепсиногенів I, II і гастрину-17 з гістологічними змінами слизової оболонки шлунку. Серологічні тести є неінвазними, точними, широкодоступними та дешевими порівняно з сучасними ендоскопічними методами. Вони є інструментом виключення і допомоги у неінвазивному виявленні атрофічного гастриту та відборі на призначення ендоскопії тим, хто має найвищий ризик.
Американська гастроентерологічна асоціація – AGA - у 2021 році (25.08. 2021) представила: Оновлення клінічної практики AGA
щодо діагностики та лікування атрофічного гастриту. Експертний огляд.
Який містить окремий розділ Серологічна діагностика, де представлені наступні тези:
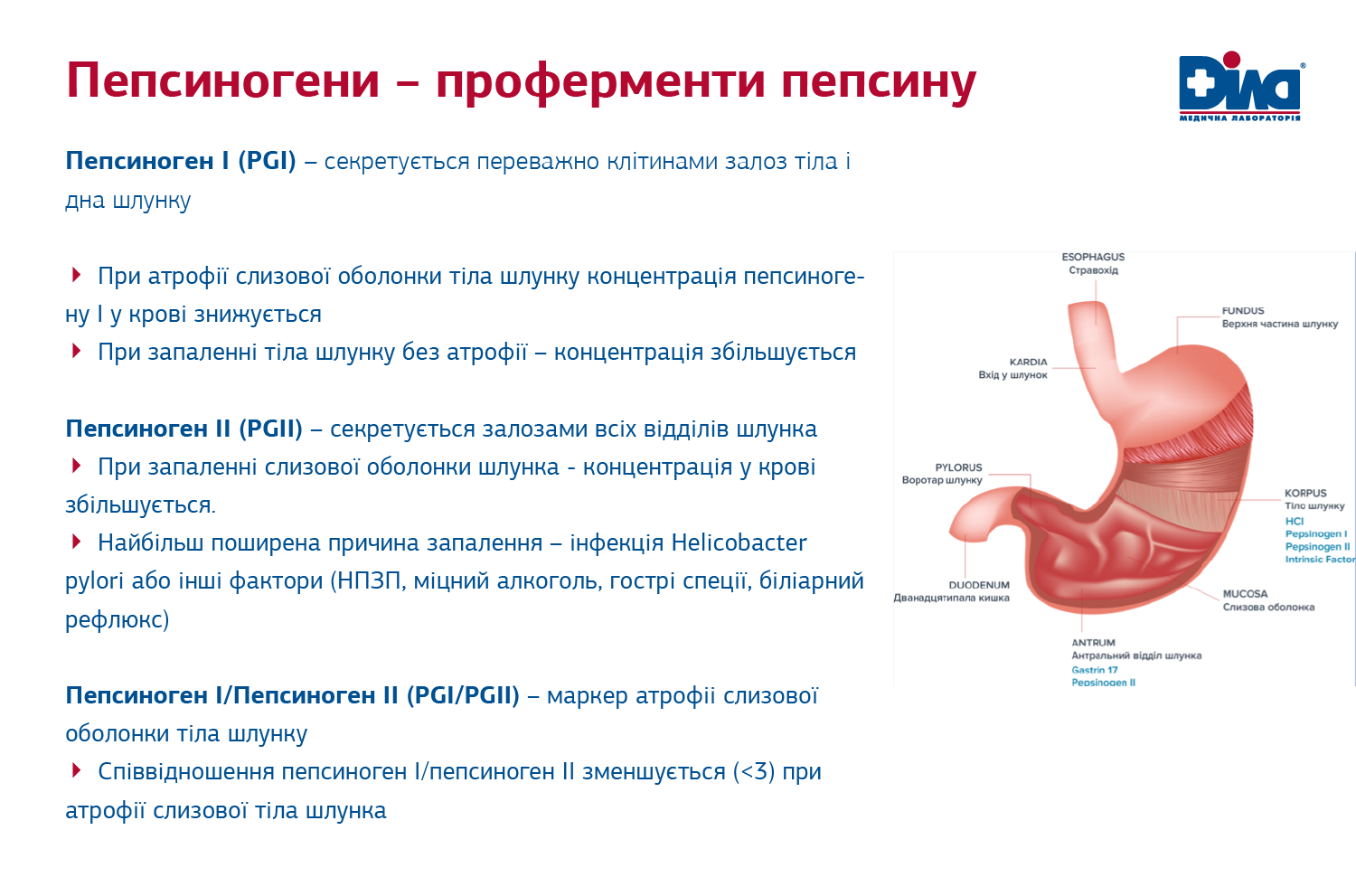
- «Сироваткові пепсиногени (ПГ) відображають як функціональний, так і морфологічний стани слизової оболонки (СО) шлунка і є корисними маркерами атрофії»
- «Головні клітини та клітини слизової оболонки шлунка та фундальних залоз секретують як ПГ I, так і ПГ II, тоді як ПГ II ( не ПГ I) також синтезується пілоричними залозами та залозами Бруннера»
- «В регіонах із високою захворюваністю на рак шлунка (з більшістю досліджень у Східній Азії) рівні PG I (<70 мкг/л) і низьке співвідношення PG I:II (<3,0) демонструють високу чутливість і специфічність для важкої атрофії СО тіла шлунка»
Вже 2 роки поспіль українські лікарі можуть отримати безоплатний доступ до платформи UpToDate, провідного глобального клінічного ресурсу доказової медицини. Платформа UpToDate містить огляди та рекомендації як для лікарів, так і для пацієнтів.
Згідно з базою даних UpToDate: щодо Лабораторної діагностики - Серології крові при ХАГ
- «Серологічне обстеження - антитіла до внутрішнього фактора, антитіла до парієтальних клітин, визначення рівня гастрину натщесерце, рекомендується як доповнення до гістологічної діагностики АМАГ»
- «Серологія (зокрема вимірювання PG I, PG II, G-17 і H. pylori - IgG) і гістологія добре узгоджуються в діагностиці атрофічного гастриту. Кореляційні дослідження
(2002р.) продемонстрували: сироваткові концентрації пепсиногенів і гастрину-17 падають зі збільшенням ступеня атрофії СО тіла та антрального відділу шлунка»
Таким чином, порівнюючи з гістологією (інвазивність, варіабельність, правдивість, чутливість, суб’єктивність, час і вартість), серологія забезпечує точні та об’єктивні підходи для оцінки стану одночасно всієї слизової оболонки шлунку з одного зразка крові.
Сьогодні в ДІЛА є низка досліджень для діагностики Хронічного Атрофічного гастриту:
Використовують для діагностики і підтвердження аутоімунного гастрита, АМАГ
- Антитіла IgG до парієтальних клітин шлунку є аутоантитілами до клітин, які виробляють соляну кислоту і внутрішній чинник Катла.
- Наявність свідчить про аутоімунний процес (атрофія слизової шлунку, порушення всмоктування вітаміну В12, розвиток перніциозної анемії)
- Гастрокомплекс ДІЛА

Це непрямий метод оцінки стану слизової оболонки шлунку по показниках крові, який не може повністю замінити гастроскопію, однак допоможе в постановці попереднього діагнозу.
Комплексне дослідження, що включає такі маркери як: пепсиноген I та II, співвідношення пепсиноген I до пепсиноген II, гастрин-17 кількісн., та Хелікобактеріоз, Helicobacter pylori, антитіла IgG. Вимірювання концентрацій перерахованих біомаркерів дозволяє провести непряму оцінку стану слизової оболонки шлунку і спланувати подальші кроки.
На підставі отриманих результатів всіх пацієнтів поділяють на три групи:
- Пацієнти з нормальною слизовою оболонкою шлунка
- Пацієнти з Хелікобактеріозом без атрофічного гастриту
- Пацієнти з атрофічним гастритом
Дослідження Гастрокомплекс використовується з метою оцінки стану слизової оболонки шлунка:
- Як метод діагностики, що дозволяє виявити причину диспепсичних розладів (нудота, печія, біль у шлунку);
- Високоспецифічний первісний метод діагностики для пацієнтів із протипоказаннями до інструментальних методів обстеження (ЕФГДС та ін.);
- Оптимальний скринінговий метод оцінки слизової оболонки шлунку та раннього виявлення атрофічного гастриту;
- Для додаткової інформації лікарю-ендоскопісту при діагностиці передракових змін слизової шлунка
Детальніше про визначення показників, що входять до Гастрокомплексу:
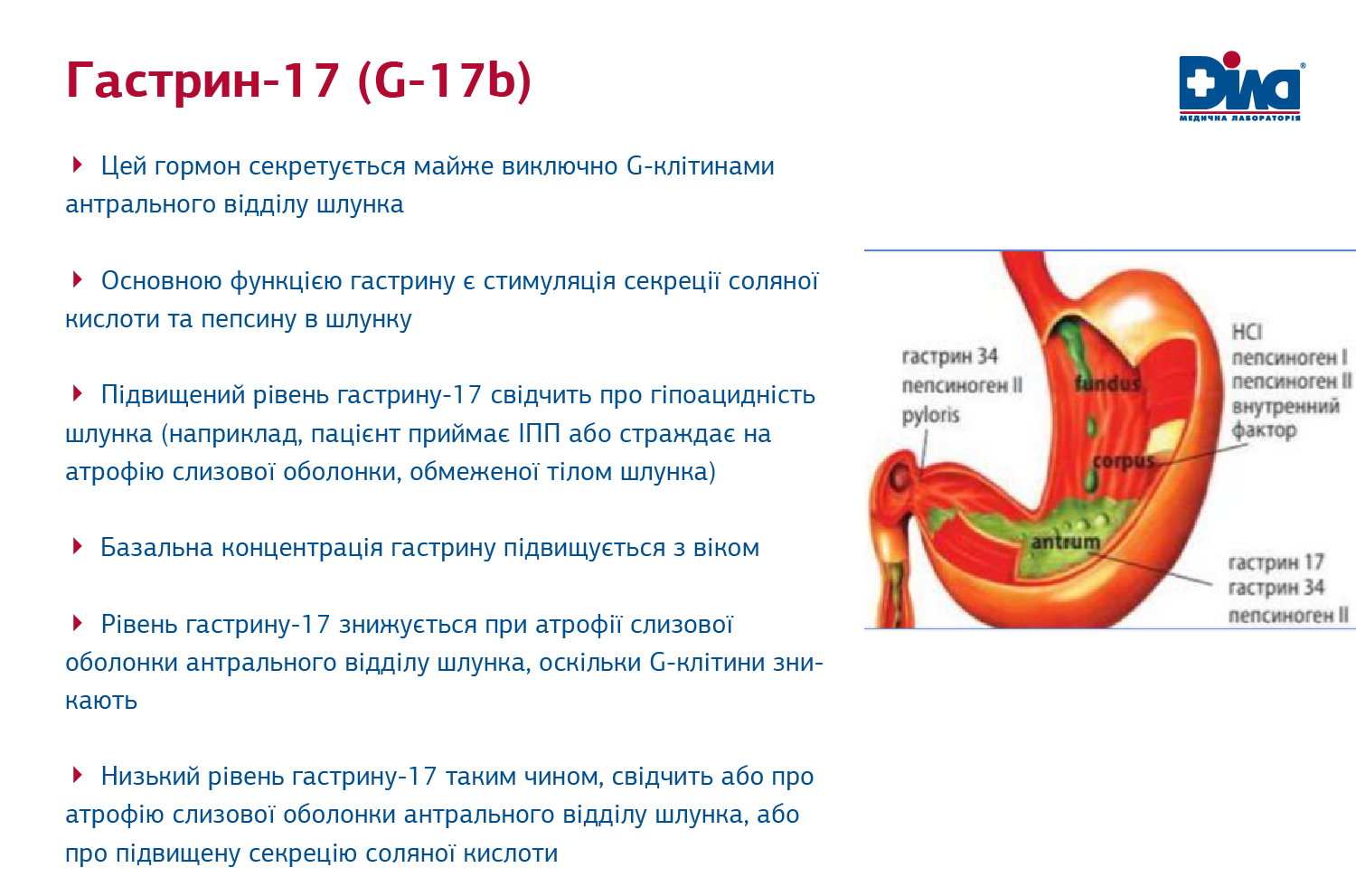
- Визначення Гастрину-17: як у складі Гастрокомплексу, так і окремо
- Визначення Хелікобактеріоз, Helicobacter pylori, антитіла IgG: як у складі Гастрокомплексу, так і окремо
Приклад: бланк заключення Гастрокомплекс - Атрофічний Пангастрит

Підсумовуючи:
- Проблема діагностики та лікування ХАГ лишається актуальною
- Необхідне чітке слідування протоколам ведення пацієнтів з метаплазією для профілактики ускладнень
- Наявність можливості неінвазивного тестування великої кількості пацієнтів з верхньоабдомінальними скаргами (Гастрокомплекс) для подальшого відбору на проведення сучасних ендоскопічних досліджень
Хронічний атрофічний гастрит (ХАГ) належить до передракових станів шлунку, на тлі цього захворювання часто розвиваються такі передракові зміни, як кишкова метаплазія і дисплазія епітелію слизової оболонки шлунку, а також гіперпроліферація її епітелію, що сприяє розвитку пухлин.
Використані джерела:
- https://www.gastrojournal.org/article/S0016-5085%2821%2903236-4/fulltext
- https://www.esge.com/management-of-epithelial-precancerous-conditions-and-lesions-in-the-stomach-maps-ii-esge-esp-sped-guideline-update-2019
- https://www.esge.com/assets/downloads/pdfs/guidelines/2019_a_0859_1883.pdf https://health-ua.com/pics/pdf/ZU_2012_Gastro_4/34-35.pdf
- Scand J Gastroenterol. 2015;50(6):657. Epub 2015 Apr 22
- Dixon M, Genta R, Yardley J, Correa P, 1996
- https://www.researchgate.net/publication/276335899_Assessment_of_Gastritis_Using_Operative_Link_for_Gastritis_Assessment_System Assessment of Gastritis Using Operative Link for Gastritis Assessment SystemSi-Hyong Jang, Kyoung-Mee KimDepartment of Pathology, Sungkyunkwan University School of Medicine, Seoul, Korea
- https://biohithealthcare.co.uk/taking-the-serological-pathway-to-endoscopy
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7767582/
- https://ar.iiarjournals.org/content/41/11/5527
- https://www.spandidos-publications.com/10.3892/etm.2021.10782
- https://www.uptodate.com/contents/gastric-cancer-screening?search=atrophic%20gastritis%20screening&source=search_result&selectedTitle=2~74&usage_type=default&display_rank=2
- https://www.uptodate.com/contents/metaplastic-chronic-atrophic-gastritis?search=atrophic%20gastritis%20screening&source=search_result&selectedTitle=6~74&usage_type=default&display_rank=6#H1047268241
- Iijima K, Abe Y, Kikuchi R, Koike T, Ohara S, Sipponen P, Shimosegawa T. Serum biomarker tests are useful in delineating between patients with gastric atrophy and normal, healthy stomach. World J Gastroenterol. 2009 Feb 21;15(7):853-9.
- Agréus L, Kuipers EJ, Kupcinskas L, Malfertheiner P, Di Mario F, Leja M, Mahachai V, Yaron N, van Oijen M, Perez Perez G, Rugge M, Ronkainen J, Salaspuro M, Sipponen P, Sugano K, Sung J. Rationale in diagnosis and screening of atrophic gastritis with stomach-specific plasma biomarkers. Scand J Gastroenterol. 2012 Feb;47(2):136-47. doi: 10.3109/00365521.2011.645501.
- Divyanshoo Rai Kohli, MD Physician, Division of Gastroenterology and Hepatology, Kansas City VA Medical Center and Coauthor(s). Achlorhydria. Updated: Mar 05, 2019. Medscape.
- Zagari RM, Rabitti S, Greenwood DC, Eusebi LH, Vestito A, Bazzoli F. Systematic review with meta-analysis: diagnostic performance of the combination of pepsinogen, gastrin-17 and anti-helicobacter pylori antibodies serum assays for the diagnosis of atrophic gastritis. Aliment Pharmacol Ther. 2017:1–11.
- Syrjänen K. A panel of serum biomarkers (GastroPanel®) in non-invasive diagnosis of atrophic gastritis. Systematic review and meta-analysis. Anticancer Res. 2016;36(10):5133–44.
- Gréus L, Kuipers EJ, Kupcinskas L, Malfertheiner P, Di Mario F, Leja M, Mahachai V, Yaron N, van Oijen M, Perez Perez G, Rugge M, Ronkainen J, Salaspuro M, Sipponen P, Sugano K, Sung J. Rationale in diagnosis and screening of atrophic gastritis with stomach-specific plasma biomarkers. Scand J Gastroenterol. 2012 Feb;47(2):136-47.
- Storskrubb T, Aro P, Ronkainen J, Sipponen P, Nyhlin H, Talley NJ, Engstrand L, Stolte M, Vieth M, Walker M, Agreus L. Serum biomarkers provide an accurate method for diagnosis of atrophic gastritis in a general population: the Kalixanda study. Scand J Gastroenterol. 2008;43(12):1448–55.
- Sipponen P, Graham DY. Importance of atrophic gastritis in diagnostics and prevention of gastric cancer: application of plasma biomarkers. Scand J Gastroenterol. 2007 Jan;42(1):2–10.
- https://www.gastropanel.com/healthcare-professionals-and-laboratories/studies
- https://www.vz.kiev.ua/atrofichnyj-gastryt-suchasnyj-poglyad/