Для перегляду доступних досліджень та термінів їх виконання

Trichomonas Vaginalis: глобальний виклик та сучасні стратегії діагностики
27.02.2026
У 2020 році Всесвітня організація охорони здоров’я (ВООЗ) оцінювала кількість нових випадків зараження Trichomonas vaginalis у віковій групі 15–49 років у 156 мільйонів на рік, при цьому близько третини інфекцій припадало на Африку та Америки1.
Епідеміологічні особливості
Trichomonas vaginalis має вищу поширеність, ніж сукупна поширеність трьох інших виліковних ІПСШ (C. trachomatis, N. gonorrhoeae та Treponema pallidum) серед жінок, що робить його провідним агентом, відповідальним за невірусні ІПСШ у світі:
- 5,3% серед жінок;
- 0,6% серед чоловіків.
Найважливішою рисою Trichomonas vaginalis є, те, що більшість інфекцій (54% за даними дослідження Lya Hamet та співавт. (2025)2) перебігають без жодних симптомів, а серед симптомних пацієнтів більшість скарг є неспецифічними – лейкорея та зуд геніталій. Такі характеристики відкривають для збудника вікно можливостей для безперешкодного і тривалого існування та розповсюдження.
Асоціація з іншими інфекціями та ризики
Trichomonas vaginalis є єдиним відомим паразитичним найпростішим що викликає ІПСШ. Він часто асоціюється з іншими збудниками (за даними Lya Hamet та співавт. (2025)2):
- 17% ‒ з C. trachomatis;
- 9,2% ‒ з M. genitalium;
- 3,6% ‒ з N. gonorrhoeae.
Наявність будь-якої інфекції, що передається статевим шляхом, має спонукати до розширеного обстеження на інші ІПСШ, включно з ВІЛ2,3. Відомо, що Trichomonas vaginalis є фактором ризику інфікування ВПЛ, вірусом простого герпесу та, що особливо важливо, ВІЛ.
Окрім симптомів з боку репродуктивного тракту, інфекція T. vaginalis часто асоціюється з наступними наслідками:
- розвитком запальних захворювань органів малого тазу;
- безпліддям;
- несприятливими наслідками вагітності (передчасним розривом плодових оболонок, передчасними пологами, низькою масою тіла новонародженого);
- підвищеним ризиком розвитку раку шийки матки.

Від колонізації до запалення: етіопатогенез трихомоніазу
Trichomonas vaginalis колонізує плоский епітелій урогенітального тракту жінок і чоловіків завдяки своїй унікальній здатності до біологічної адаптації:
- Механізм пошкодження: руйнує епітеліальні клітини шляхом вивільнення цитотоксичних речовин, індукції запалення та порушення вагінального мікробіому.
- Ухилення від імунітету: антигенна варіабельність поверхневих структур, продукція протеолітичних ферментів і здатність до утворення біоплівок.
- Фактор pH: для встановлення інфекції збудник потребує вагінального pH у межах 5,0–5,5 (у нормі ‒ 4,0–4,5). Через це дівчата препубертатного віку та жінки в менопаузі (де pH наближається до 7,0) менш сприйнятливі до інфекції.
Шляхи передачі та фактори ризику
Сексуально активні люди зазвичай інфікуються трихомоніазом під час пенільно-вагінального статевого контакту з партнером, що має трихомоніаз, незалежно від наявності клінічних проявів. Новонароджені можуть інфікуватися під час проходження через інфіковані пологові шляхи при вагінальних пологах і розвивати симптоми протягом перших 3–4 тижнів життя.
До факторів ризику інфікування належать:
- наявність кількох статевих партнерів;
- незахищені статеві контакти;
- анамнез інших інфекцій, що передаються статевим шляхом (ІПСШ);
- використання внутрішньоматкових контрацептивів;
- спільне використання секс-іграшок без належного очищення або захисту.
Інші чинники, зокрема куріння, бідність, низький рівень освіти та перебування в місцях позбавлення волі, також асоціюються з вищою поширеністю інфекції.
Сучасні підходи до лабораторної діагностики трихомоніазу
Симптоми та клінічні ознаки трихомоніазу не є достатньо чутливими або специфічними для встановлення діагнозу, на відміну від деяких інших інфекцій, що передаються статевим шляхом. Симптомні жінки зазвичай скаржаться на неприємний запах вагінальних виділень, біль, свербіж та/або подразнення вульви та піхви. При огляді іноді можливо виявити патогномонічні ознаки – пінисті виділення та «полуничну шийку» що характеризується точковими геморагічними ураженнями слизової. Але останні десятиліття ці класичні симптоми є скоріше виключенням ніж закономірністю. У чоловіків можуть виникати скарги на болісне сечовипускання, розвиватись простатит або епідидиміт. Для підтвердження наявності збудника необхідна лабораторна діагностика.
Еволюція діагностичних методів
|
Метод |
Характеристики та чутливість |
Обмеження |
|
Мікроскопія (нативний мазок) |
Чутливість 44–68%. |
Низька ефективність; провокаційні методи більше не рекомендовані. |
|
Культивування (середовище Diamond) |
Чутливість 81–94%. |
Тривалий час очікування; ризик контамінації флорою. |
|
Система InPouch® TV |
Дозволяє одночасну мікроскопію та культивування. |
Потребує виключно життєздатних збудників у зразку. |
|
МАНК (ПЛР) |
«Золотий стандарт». Найвища чутливість та специфічність. |
Потребує таргетування консервативних ділянок (напр., бета-тубулін). |
Діагностика на ранніх етапах розвитку медицини ґрунтувалася на прямому виявленні рухомих трофозоїтів у нативних мазках з вагінального секрету або уретри, та мала низьку чутливість (44–68%). Для збільшення шансів виявлення Trichomonas vaginalis застосовувалися провокаційні методи, що нині не рекомендовані жодним сучасним клінічним гайдлайном. До впровадження тестів ампліфікації нуклеїнових кислот першою лінією діагностики T. vaginalis вважалося культивування в середовищі Diamond, чутливість якого становила 81–94%, що нівелювалось частою контамінацією вагінальною бактеріальною флорою, залежністю від життєздатності збудника та тривалим часом отримання результатів дослідження.
Для мінімізації ризику контамінації були розроблені культуральні системи, зокрема система InPouch® (BioMed Diagnostics, White City, OR), у якій зразок розміщується в двокамерному пакеті, що дозволяє одночасно проводити дослідження нативного препарату та культивування. Недоліком дослідження є потреба у життєздатних збудниках – якщо збудник не життєздатний, культура не дасть позитивного результату, хоча інфекція могла бути присутня ‒ це обмежує чутливість у певних випадках. Цей метод був золотим стандартом до впровадження методів ампліфікації нуклеїнових кислот (МАНК), яким він хоч і передав цей «титул», дотепер залишається надзвичайно важливим елементом діагностики.
МАНК, зокрема полімеразна ланцюгова реакція (ПЛР), характеризуються високою чутливістю та специфічністю та є «золотим стандартом» лабораторного виявлення інфекції. Водночас T. vaginalis має генетичні особливості що певною мірою забезпечують їй «невловимість». Генетична варіабельність у ділянках, які таргетуть ПЛР-набори може зменшувати чутливість ПЛР, особливо якщо з’являються мутації у місці праймерів, водночас сучасні набори ПЛР розроблені з урахуванням цього явища та таргетують консервативні ділянки геному, як, бета-тубулін. Бета-тубулін має характерну послідовність у T. vaginalis, оскільки він разом з альфа-тубуліном утворює мікротрубочки — основну структуру цитоскелету та джгутиків у Trichomonas vaginalis, що критично необхідні для руху та поділу мікроорганізму.
Генетичний поліморфізм T. vaginalis
Геном T. vaginalis є великим у порівнянні з іншими патогенами і становить близько 160 мільйонів пар основ з великою кількість повторів та транспозонів, а також містить приблизно 60 000 білок-кодуючих генів. Така велика кількість генетичного матеріалу зумовлює генетичний поліморфізм, варіабельність та високі адаптаційні можливості, що є першоджерелом широкого спектру як медичних наслідків, так і ускладнень.
Генетична варіабельність може впливати на клінічні та патологічні прояви T. vaginalis. Перехід від мікроскопічної до молекулярної діагностики (ПЛР) дав краще розуміння епідеміології та генетичного різноманіття T. vaginalis. Наразі виявлено два основні генотипи T. Vaginalis:
- Генотип І. Більш древній, висока варіабельність, виражений інфекційний процес.
- Генотип ІІ. Асоціюється з резистентністю до метронідазолу – антибіотика першої лінії лікування.
У популяції вони виявляються приблизно в однаковому співвідношенні.
Вивчення генетичної спорідненості між клінічними зразками, дозволяє відстежувати шляхи передачі інфекції, спалахи захворювання, а також відрізняти неефективність лікування від повторного інфікування.
Водночас генетична варіабельність та еволюціонування T. vaginalis може становити проблему для ПЛР діагностики. Саме тому діагностика трихомоніазу має бути комплексною і синдромальною. Комплексність полягає у застосуванні як ПЛР так і бак посіву InPouch TV, з урахуванням клінічних проявів. Оскільки T. vaginalis часто поєднується з іншими ІПСШ, а при бактервіальному вагінозі ‒ 25% жінок мають коінфекцію з ІПСШ, важливо тестувати на інших збудників ІПСШ щоб поліпшити результати виліковування.
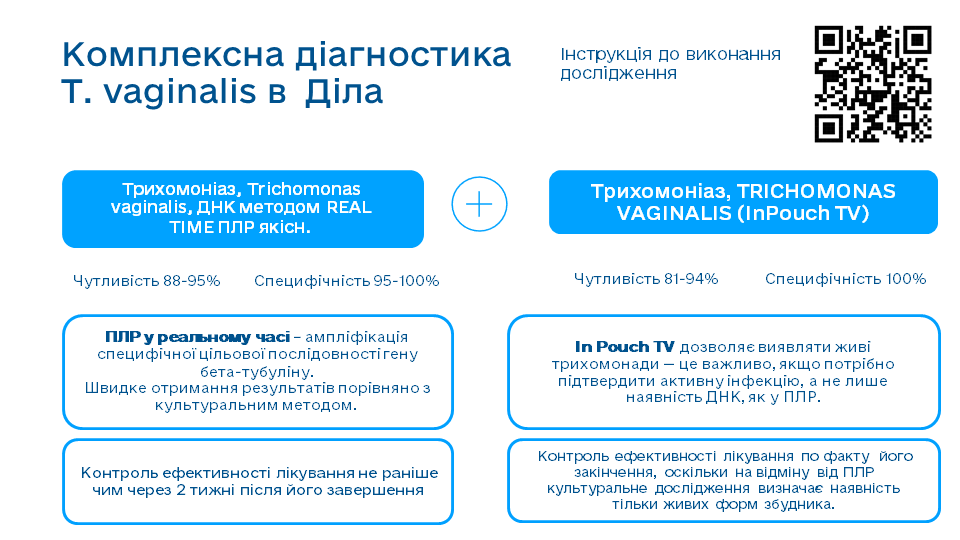
Контроль вилікуваності та комплексний підхід
Контроль вилікуваності (test of cure) є обов’язковим для для всіх ІПСШ через як мінімум 21 день після закінчення терапії. Цей проміжок необхідний для виключення позитивних результатів ПЛР в результаті взаємоії з генетичним матеріалом зруйнованих мікроорганізмів. При трихомоніазі застосування культурального методу InPouchTV дозволяє провести контроль вилікуваності невдовзі після закінчення терапії і таким чином виявити її можливу неефективність або реінфекцію.
Діагностичні рішення від ДІЛА
ДІЛА пропонує наступні дослідження для вирішення діагностичної задачі виявлення трихомоніазу:
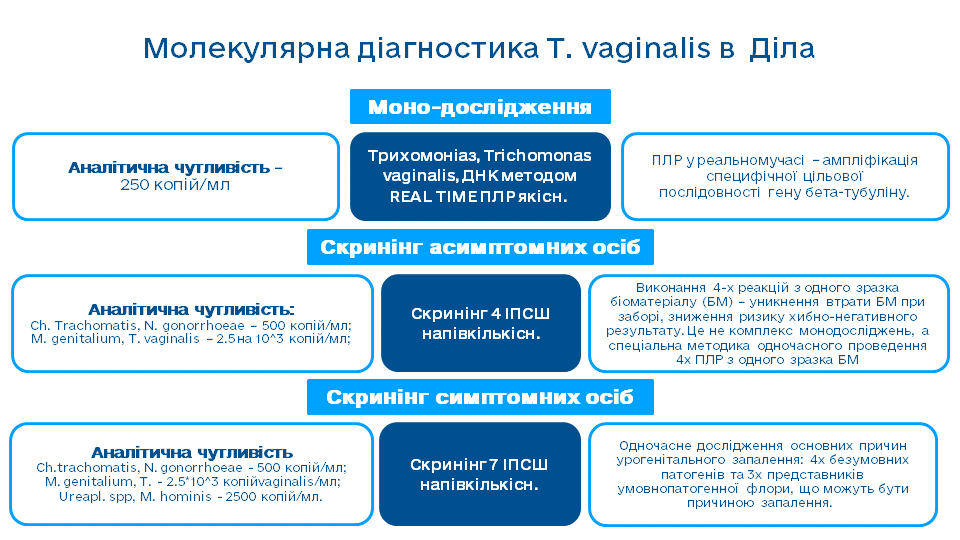
- Трихомоніаз, Trichomonas vaginalis, ДНК методом REAL TIME ПЛР - якісн.
- Скринінг 4 ІПСШ - напівкількісн.
- Скринінг 7 ІПСШ - напівкількісн.
- Трихомоніаз, TRICHOMONAS VAGINALIS (InPouch TV)
- Комплекс №168 "Партнерська турбота (розширений)"
До складу діагностики аномальних вагінальних виділень відповідно до СМД «Аномальні вагінальні виділення» входять:
- Мікроскопія вагінальних виділень за критеріями Хей-Айсон та шкалою Nugent
- Бак. посів урогенітальних виділень (1 точка) з антибіотикограмою ДДМ
Переваги ДІЛА
- ПЛР-аналізи на інфекції, що передаються статевим шляхом, у лабораторії ДІЛА виконуються з високою точністю та надійністю завдяки власній системі управління якістю та міжнародній акредитації ISO 15189.
- Усе обладнання та реагенти ДІЛА мають маркування IVD, проходять регулярний аудит, звітність та калібрування.
- Для зручності пацієнтів доступні консультації фахівців кол-центру. Професійний забір біоматеріалу у відділенні дозволяє швидко отримати результати аналізів.
- ДІЛА дотримується принципів доказової медицини, тому скринінг ІПСШ методом ПЛР, що є молекулярною діагностикою, визнаний золотим стандартом у світі. Такий підхід робить діагностику надійною, комфортною, безпечною та оперативною
- https://www.who.int/en/news-room/fact-sheets/detail/trichomoniasis
- Hamet, Lya et al. “Prevalence and bio-clinical characterisation of Trichomonas vaginalis infection in a large cohort of French patients screened using a molecular syndromic panel for sexually transmitted infections.” The Journal of infection vol. 91,4 (2025): 106610. doi:10.1016/j.jinf.2025.106610
- Стандарти медичної допомоги «Аномальні вагінальні виділення» ГС 2022-2264 від 15.12.2022