Trichomonas Vaginalis: глобальный вызов и современные стратегии диагностики
27.02.2026
В 2020 году Всемирная организация здравоохранения (ВОЗ) оценивала количество новых случаев заражения Trichomonas vaginalis в возрастной группе 15–49 лет в 156 миллионов в год, при этом около трети инфекций приходилось на Африку и Америку1.
Эпидемиологические особенности
Trichomonas vaginalis имеет более высокую распространенность, чем совокупная распространенность трех других излечимых ИППП (C. trachomatis, N. gonorrhoeae и Treponema pallidum) среди женщин, что делает его ведущим агентом, ответственным за невирусные ИППП в мире
- 5,3% среди женщин;
- 0,6% среди мужчин.
Важнейшей особенностью Trichomonas vaginalis является то, что большинство инфекций (54% по данным исследования Lya Hamet и соавт. (2025)2) протекают без каких-либо симптомов, а среди симптоматических пациентов большинство жалоб являются неспецифическими – лейкорея и зуд гениталий. Такие характеристики открывают для возбудителя окно возможностей для беспрепятственного и длительного существования и распространения.
Ассоциация с другими инфекциями и риски
Trichomonas vaginalis является единственным известным паразитическим простейшим, вызывающим ИППП. Он часто ассоциируется с другими возбудителями (по данным Lya Hamet и соавт. (2025)2):
- 17% ‒ с C. trachomatis;
- 9,2% ‒ с M. genitalium;
- 3,6% ‒ с N. gonorrhoeae.
Наличие любой инфекции, передаваемой половым путем, должно побудить к расширенному обследованию на другие ИППП, включая ВИЧ2,3. Известно, что Trichomonas vaginalis является фактором риска инфицирования ВПЧ, вирусом простого герпеса и, что особенно важно, ВИЧ.
Кроме симптомов со стороны репродуктивного тракта, инфекция T. vaginalis часто ассоциируется со следующими последствиями:
- развитием воспалительных заболеваний органов малого таза;
- бесплодием;
- неблагоприятными последствиями беременности (преждевременным разрывом плодных оболочек, преждевременными родами, низкой массой тела новорожденного);
- повышенным риском развития рака шейки матки.

От колонизации до воспаления: этиопатогенез трихомониаза
Trichomonas vaginalis колонизирует плоский эпителий урогенитального тракта женщин и мужчин благодаря своей уникальной способности к биологической адаптации:
- Механизм повреждения: разрушает эпителиальные клетки путем высвобождения цитотоксических веществ, индукции воспаления и нарушения вагинального микробиома.
- Уклонение от иммунитета: антигенная вариабельность поверхностных структур, продукция протеолитических ферментов и способность к образованию биопленок.
- Фактор pH: для установления инфекции возбудитель нуждается в вагинальном pH в пределах 5,0–5,5 (в норме — 4,0–4,5). Из-за этого девушки препубертатного возраста и женщины в менопаузе (где pH приближается к 7,0) менее восприимчивы к инфекции.
Пути передачи и факторы риска
Сексуально активные люди обычно инфицируются трихомониазом во время пенильно-вагинального полового контакта с партнером, имеющим трихомониаз, независимо от наличия клинических проявлений. Новорожденные могут инфицироваться во время прохождения через инфицированные родовые пути при вагинальных родах и развивать симптомы в течение первых 3–4 недель жизни.
К факторам риска инфицирования относятся:
- наличие нескольких половых партнеров;
- незащищенные половые контакты;
- анамнез других инфекций, передаваемых половым путем (ИППП);
- использование внутриматочных контрацептивов;
- совместное использование секс-игрушек без надлежащей очистки или защиты.
Другие факторы, в частности курение, бедность, низкий уровень образования и пребывание в местах лишения свободы, также ассоциируются с более высокой распространенностью инфекции.
Современные подходы к лабораторной диагностике трихомониаза
Симптомы и клинические признаки трихомониаза не являются достаточно чувствительными или специфическими для установления диагноза, в отличие от некоторых других инфекций, передаваемых половым путем. Симптоматические женщины обычно жалуются на неприятный запах вагинальных выделений, боль, зуд и/или раздражение вульвы и влагалища. При осмотре иногда можно обнаружить патогномоничные признаки – пенистые выделения и «клубничную шейку», характеризующуюся точечными геморрагическими поражениями слизистой. Но в последние десятилетия эти классические симптомы являются скорее исключением, чем закономерностью. У мужчин могут возникать жалобы на болезненное мочеиспускание, развиваться простатит или эпидидимит. Для подтверждения наличия возбудителя необходима лабораторная диагностика.
Эволюция диагностических методов
|
Метод |
Характеристики и чувствительность |
Ограничение |
|
Микроскопия (нативный мазок) |
Чувствительность 44–68%. |
Низкая эффективность; Провокационные методы больше не рекомендованы. |
|
Культивирование (среда Diamond) |
Чувствительность 81–94%. |
Долгое время ожидания; риск контаминации флорой. |
|
Система InPouch® TV |
Позволяет одновременную микроскопию и культивирование. |
Нуждается исключительно в жизнеспособных возбудителях в образце. |
|
МОНК (ПЦР) |
«Золотой стандарт». Высокая чувствительность и специфичность. |
Нуждается в таргетировании консервативных участков (напр., бета-тубулин). |
Диагностика на ранних этапах развития медицины основывалась на прямом выявлении подвижных трофозоитов в нативных мазках из вагинального секрета или уретры и имела низкую чувствительность (44–68%). Для увеличения шансов выявления Trichomonas vaginalis применялись провокационные методы, которые в настоящее время не рекомендуются ни одним современным клиническим гайдлайном. До внедрения тестов амплификации нуклеиновых кислот первой линией диагностики T. vaginalis считалось культивирование в среде Diamond, чувствительность которого составляла 81–94%, что нивелировалось частой контаминацией вагинальной бактериальной флорой, зависимостью от жизнеспособности возбудителя и длительным временем получения результатов исследования.
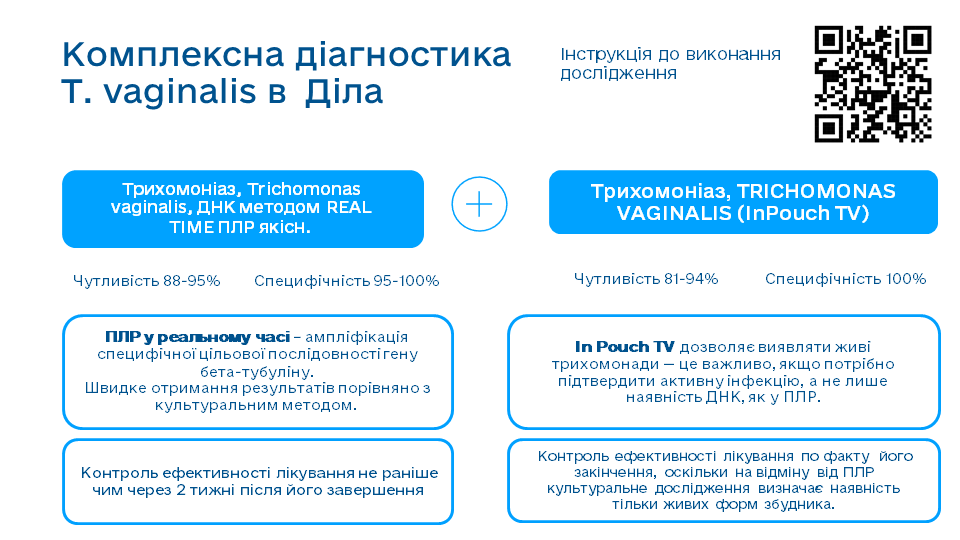
Для минимизации риска контаминации были разработаны культуральные системы, в частности система InPouch® (BioMed Diagnostics, White City, OR), в которой образец помещается в двухкамерный пакет, что позволяет одновременно проводить исследование нативного препарата и культивирование. Недостатком исследования является необходимость в жизнеспособных возбудителях — если возбудитель не жизнеспособен, культура не даст положительного результата, хотя инфекция могла присутствовать — это ограничивает чувствительность в определенных случаях. Этот метод был золотым стандартом до внедрения методов амплификации нуклеиновых кислот (МАНК), которым он хоть и передал этот «титул», до сих пор остается чрезвычайно важным элементом диагностики.
МАНК, в частности полимеразная цепная реакция (ПЦР), характеризуются высокой чувствительностью и специфичностью и являются «золотым стандартом» лабораторного выявления инфекции. В то же время T. vaginalis имеет генетические особенности, которые в определенной степени обеспечивают ей «неуловимость». Генетическая вариабельность в участках, которые таргетируют ПЦР-наборы, может уменьшать чувствительность ПЦР, особенно если появляются мутации в месте праймеров, в то же время современные наборы ПЦР разработаны с учетом этого явления и таргетируют консервативные участки генома, такие как бета-тубулин. Бетатубулин имеет характерную последовательность в T. vaginalis, поскольку он вместе с альфа-тубулином образует микротрубочки — основную структуру цитоскелета и жгутиков в Trichomonas vaginalis, которые критически необходимы для движения и деления микроорганизма.
Генетический полиморфизм T. vaginalis
Геном T. vaginalis является большим по сравнению с другими патогенами и составляет около 160 миллионов пар оснований с большим количеством повторов и транспозонов, а также содержит примерно 60 000 белко-кодирующих генов. Такое большое количество генетического материала обусловливает генетический полиморфизм, вариабельность и высокие адаптационные возможности, что является первоисточником широкого спектра как медицинских последствий, так и осложнений.
Генетическая вариабельность может влиять на клинические и патологические проявления T. vaginalis. Переход от микроскопической к молекулярной диагностике (ПЦР) дал лучшее понимание эпидемиологии и генетического разнообразия T. vaginalis. В настоящее время выявлено два основных генотипа T. Vaginalis:
- Генотип I. Более древний, высокая вариабельность, выраженный инфекционный процесс.
- Генотип II. Ассоциируется с резистентностью к метронидазолу – антибиотику первой линии лечения.
В популяции они встречаются примерно в равном соотношении.
Изучение генетического сходства между клиническими образцами позволяет отслеживать пути передачи инфекции, вспышки заболевания, а также отличать неэффективность лечения от повторного инфицирования.
В то же время генетическая вариабельность и эволюционирование T. vaginalis может представлять проблему для ПЦР-диагностики. Именно поэтому диагностика трихомониаза должна быть комплексной и синдромальной. Комплексность заключается в применении как ПЦР, так и бак посева InPouch TV, с учетом клинических проявлений. Поскольку T. vaginalis часто сочетается с другими ИППП, а при бактериальном вагинозе ‒ 25% женщин имеют коинфекцию с ИППП, важно тестировать на других возбудителей ИППП, чтобы улучшить результаты лечения.
Контроль излечения и комплексный подход
Контроль излечения (test of cure) является обязательным для всех ИППП через минимум 21 день после окончания терапии. Этот промежуток необходим для исключения положительных результатов ПЦР в результате взаимодействия с генетическим материалом разрушенных микроорганизмов. При трихомониазе применение культурального метода InPouchTV позволяет провести контроль излечения вскоре после окончания терапии и таким образом выявить ее возможную неэффективность или реинфекцию.
Диагностические решения от ДІЛА
ДІЛА предлагает следующие исследования для решения диагностической задачи выявления трихомониаза:
- Трихомониаз, Trichomonas vaginalis, ДНК методом REAL TIME ПЦР - качественный.
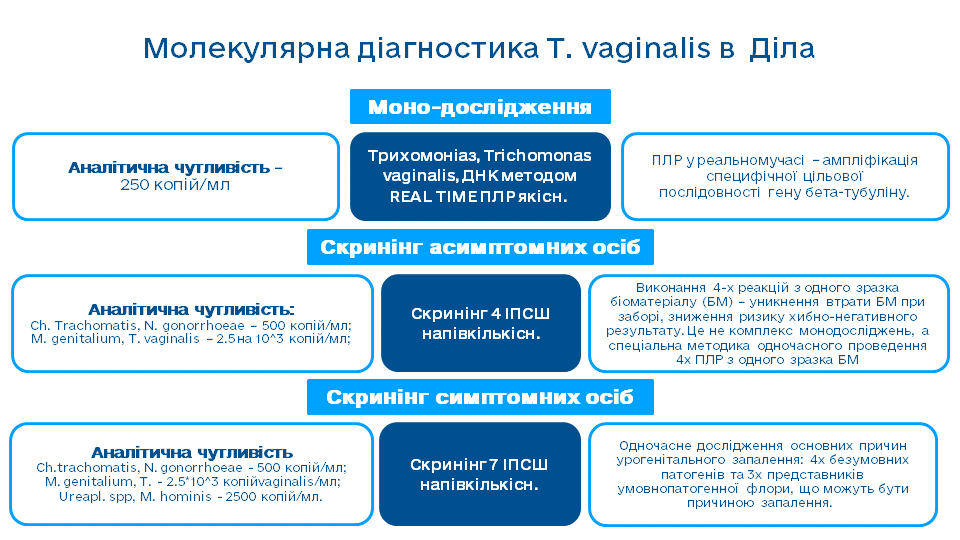
- Скрининг 4 ИППП - полуколичественный.
- Скрининг 7 ИППП - полуколичественный.
- Трихомониаз, TRICHOMONAS VAGINALIS (InPouch TV)
- Комплекс №168 «Партнерская забота (расширенный)"
В состав диагностики аномальных вагинальных выделений в соответствии с СМД «Аномальные вагинальные выделения» входят входять:
- Микроскопия вагинальных выделений по критериям Хей-Айсон и шкале Nugent
- Бак. посев урогенитальных выделений (1 точка) с антибиотикограммой ДДМ
Преимущества ДІЛА
- ПЦР-анализы на инфекции, передающиеся половым путем, в лаборатории ДІЛА выполняются с высокой точностью и надежностью благодаря собственной системе менеджмента качества и международной аккредитации ISO 15189.
- Все оборудование и реагенты ДІЛА имеют маркировку IVD, проходят регулярный аудит, отчетность и калибровку.
- Для удобства пациентов доступны консультации специалистов колл-центра. Профессиональный сбор биоматериала в отделении позволяет быстро получить результаты анализов.
- ДІЛА соблюдает принципы доказательной медицины, поэтому скрининг ИППП методом ПЦР, являющейся молекулярной диагностикой, признан золотым стандартом в мире. Такой подход делает диагностику надежной, комфортной, безопасной и оперативной
- https://www.who.int/en/news-room/fact-sheets/detail/trichomoniasis
- Hamet, Lya et al. “Prevalence and bio-clinical characterisation of Trichomonas vaginalis infection in a large cohort of French patients screened using a molecular syndromic panel for sexually transmitted infections.” The Journal of infection vol. 91,4 (2025): 106610. doi:10.1016/j.jinf.2025.106610
- Стандарты медицинской помощи «Аномальные влагалищные выделения» ГС 2022-2264 от 15.12.2022