Для перегляду доступних досліджень та термінів їх виконання

25 травня - Всесвітній день щитоподібної залози (World Thyroid Day)
21.05.2025
З прадавніх часів людству відома важлива роль щитоподібної залози в забезпеченні життєдіяльності організму.
Перші спостереження щодо зоба описано вже близько 3600 років до н.е. в китайських медичних працях. Однак, перша можливість лабораторного дослідження функції щитоподібної залози з’явилася лише в 1963 р., коли Кондліфф очистив тиреотропін та надалі разом з Оделлом та Ютігером повідомив про перше імунологічне дослідження людського тиреотропіну.
А в 1970 р. Браверман, Інгбар та Стерлінг описали, що ендогенний трийодтиронін утворюється з тироксину. З тих пір, завдяки швидкому та прогресивному розвитку тиреоїдології, накопичено значний пул знань щодо ведення патології щитоподібної залози.
Для підвищення рівня інформованості суспільства про сучасні можливості діагностики, профілактики та лікування захворювань щитоподібної залози в 2009 році, з ініціативи Європейської тиреоїдної асоціації, 25-го травня щорічно відзначається Всесвітній день щитоподібної залози (World Thyroid Day).
Сучасні можливості рішення клінічної задачі «Оцінка функціонального стану щитоподібної залози»
Нижче наведено історичні події у вивченні функції щитоподібної залози:
- 1786 рік, Калеб Хіллер Паррі, лікар з міста Бат, Англія, був першою людиною, яка описала ознаки гіпертиреозу а в 1840, Адольф фон Базедов (Німеччина), описав токсичний зоб.
- 1880 р. Людвіг Рен (Німеччина) провів першу тиреоїдектомію пацієнту з хворобою Грейвса та в 1888 році Лондонське клінічне товариство пов'язало кретинізм, мікседему, «кретинічноподібний» стан після тиреоїдектомії з одним і тим же захворюванням, пізніше відомим як гіпотиреоз.
- Вже в 1891 році Мюррей вперше описав лікування гіпотиреозу екстрактом щитоподібної залози.
- 1909, Теодор Кохер отримав Нобелівську премію з фізіології та медицини за роботу з фізіології, патології та хірургії щитоподібної заолози.
- 1912 рік, Хакару Хашимото, японський лікар, вперше описав тиреоїдит Хашимото.
- Опис синтезу тироксину відбувся в 1927р (Харінгтон і Баргер), а в 1943 р. Аствуд описав тіоурацил для лікування гіпертиреозу. В 1952 р винайдено Карбімазол винайдено в 1952р, а Гросс і Пітт-Ріверс відкрили трийодтиронін.
- 1956 р. Ройтт та його колеги повідомили про наявність циркулюючих тиреоїдних аутоантитіл при тиреоїдиті Хашимото.
- 1970 р. Браверман, Інгбар та Стерлінг описали, що ендогенний трийодтиронін утворюється з тироксину.
Сучасний алгоритм лабораторної оцінки функції щитоподібної залози є наступним:
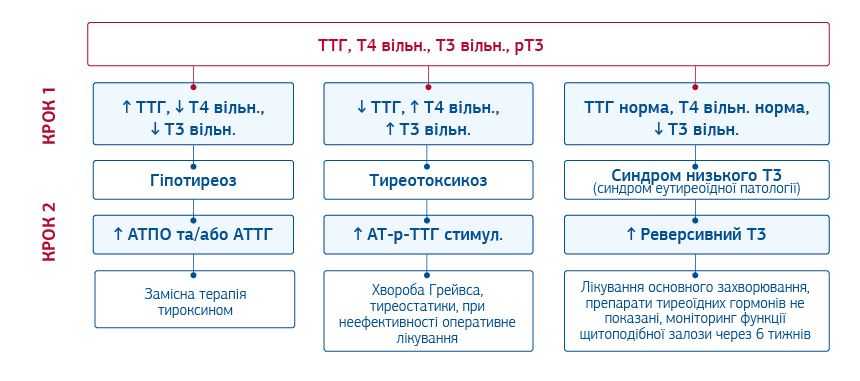
Алгоритм 1.
Таким чином, при класичних змінах співвідношення ТТГ, вТ4, вТ3, виявлення АТПО та / або АТТГ підтверджує наявність автоімунного тиреоїдиту.
Якщо ж співвідношення ТТГ, вТ4, вТ3 є неочікуваним (дискордантність показників), дослідження рівня реверсивного Т3 дозволяє диференціювати істинний гіпотиреоз від синдрому нетиреоїдної патології.
При змінах рівнів ТТГ, вТ4, вТ3, характерних для тиреотоксикозу, підвищений рівень маркеру «Антитіла до рецепторів ТТГ», а саме фракції стимулюючих антитіл, дозволяє встановити хворобу Грейвса, як причину тиреотоксикозу, та надалі проводити точний, достовірний моніторинг лікування.
Вимоги медичних керівництв щодо лабораторної діагностики та моніторингу у випадку наявності додаткового утворення в ділянці щитоподібної залози
Вогнищевим утворенням в ділянці щитоподібної залози може бути доброякісний вузол щитоподібної залози, рак, псевдовузол або аденома/гіперплазія прищитоподібної (прищитоподібних) залоз. Для рішення клінічної задачі «Скринінг при вогнищевому утворенні в ділянці щитоподібної залози» регламентовано наступні лабораторні дослідження
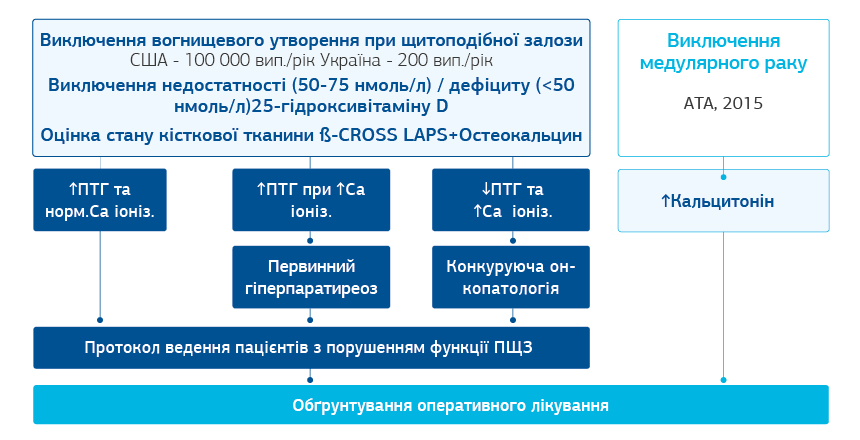
Алгоритм 2.
У випадку медулярного раку можливим є застосування маркерів Кальцитонін+Прокальцитонін+Хромогранін разом на доопераційному етапі (та/або проведення тесту стимуляції кальцієм) та дослідження рівнів цих маркерів разом з рівнем РЕА в післяопераційному періоді.
Йод та селен. Кому, коли, скільки?
Ще на початку 13 століття ендемічний кретинізм був відзначений в альпійській Європі, а в 16 столітті Парацельс першим згадав про співіснування ендемічного зобу та кретинізму в герцогстві Зальцбург.
Тироксин та трийодтиронін містять йод, тому при дефіциті йоду щитоподібна залоза збільшується, але не може синтезувати достатню кількість гормонів.
У щитоподібній залозі може запасатися до 16 мг йоду. Залежно від віку добова потреба в йоді складає від 90 до 300 мкг, українці щодня споживають лише 40–80 мкг йоду на добу (найменше: - Західна Україна та Чернігівська область).
Найпростішою профілактикою дефіциту йоду в організмі є споживання йодованої солі та продуктів з високим вмістом йоду (морепродукти, біла риба, ламінарія, овочі, фрукти, яйця, молоко, яловичина, волоські горіхи). За все життя людина споживає близько 3–5 г йоду - приблизно одну чайну ложку.
В 1980 році Всесвітня організація охорони здоров'я вперше опублікувала глобальну оцінку поширеності йододефіциту та зобу, на який страждає від 20 до 60% населення світу (переважно в країнах, що розвиваються).
В Україні патологія щитоподібної залози складає 47% від усіх ендокринопатій. Збагачення кухонної солі йодом розпочалося вперше у Швейцарії у 1922 році, однак і наразі програми профілактики йододефіциту відсутні у багатьох країнах.
На сучасному етапі показання для застосування препаратів йоду наступні:
- недостатнє надходження йоду в організм;
- ендемічний зоб у людей, які проживають у районах з дефіцитом йоду;
- зоб після резекції;
- лікування йододефіциту та дифузного еутиреоїдного зоба у немовлят, дітей, підлітків та у дорослих.
Враховуючи, що в рутинній практиці відсутні індивідуальні маркери йододефіциту, а вимірювання рівня йоду в сечі та / або Тиреоглобуліну регламентовані лише для популяційних досліджень, для прийняття рішення щодо призначення препаратів йоду слід оцінити стан щитоподібної залози (алгоритм 1, алгоритм 2), враховуючи протипоказання та супутні стани:
- маніфестний гіпертиреоз/латентний гіпертиреоз - не призначати йод в дозах ≥ 150 мкг на добу;
- автономна аденома/фокальні та дифузні вогнища автономії щитоподібної залози-при дозах 300-1000 мкг йоду на добу може розвинутись гіпертиреоз, індукований йодом – не призначати, за виключенням передопераційної йодотерапії з метою блокади щатоподібної залози за Пламером;
- стан перед лікуванням/під час лікування гіпертиреозу - уникати будь-якого прийому йоду (дефіцит йоду підвищує, а надлишок його знижує реакцію на терапію гіпертиреозу тиреостатичними засобами);
- вагітність, лактація - не призначати йод в міліграмному діапазоні (йод проходить через плаценту, плод чутливий до фармакологічно активних доз йоду), особливо при лактації, оскільки концентрація йоду в молоці (також у слині, у шлунковому соку) у 30 разів вища, ніж у крові. Виключення: високодозована йодна профілактика, після ядерно-технічних аварій.
Щодо надлишку йоду, ВООЗ вважає безпечною дозу йоду в 1 000 мкг (1 мг) на добу. При призначенні препаратів йоду слід пам’ятати, що вплив йоду може відбуватися через йодовмісні речовини. Такі агенти як дезінфікуючі засоби, аміодарон, рентгенологічні контрастні речовини та місцеві антисептики (повідон-йод та інші) можуть бути зобогенними, тому що містять кількість йоду, яка у кілька тисяч разів перевищує його вміст в природних харчових продуктах та препаратах для профілактики /лікування йододефіциту. Паління цигарок пов’язане з високою концентрацією тіоціанату в плазмі крові, який може конкурувати з йодом за поглинання щитоподібною залозою.
Селен – мікроелемент, необхідний для синтезу білків-селенопротеїнів. Згідно з наказом МОЗ України № 1073 від 03.09.2017 р. «Про затвердження Норм фізіологічних потреб населення України в основних харчових речовинах і енергії» рекомендована кількість селену для чоловіків становить 70 мкг/добу, для жінок – 50 мкг/добу; в період вагітності та лактації, а також для жінок похилого віку – 70 мкг/добу. Основними джерелами селену є м’ясні продукти та риба, неорганічні форми (селеніт і селенат) є компонентами харчових добавок.
Вважається, що близько 15% населення планети страждає на дефіцит селену, внаслідок недостатнього надходження з їжею та впливу токсичних речовин (свинцю, кадмію, ртуті, миш’яку, алюмінію), що порушує всмоктування селену.
Щитоподібна залоза містить найбільшу кількість селену на грам тканини. При недостатності селену відбувається зниження синтезу селенопротеїнів (йодотироніндейодиназ, які відповідають за перетворення тироксину в біологічно активну форму трийодтиронін), також знижується активність глутатіонпероксидази, пероксид водню накопичується в тканині ЩЗ, що спричиняє ушкодження тироцитів. У значній кількості досліджень вивчено вплив додаткового прийому селену на перебіг різних захворювань ЩЗ (насамперед - автоімунного тиреоїдиту, хвороби й орбітопатії Грейвса, виявлено що в осіб з раком ЩЗ рівень селену та магнію є нижчим, а рівень міді – вищим, ніж у здорових людей (F. Shen і співавт. (2015).
Виявлено, що селен може знижувати концентрацію АТПО, однак це зниження спостерігалося не в усіх. Суперечливі дані щодо добавок селену роблять будь-які узагальнені рекомендації ненадійними, особливо для регіонів з різним споживанням йоду, селену або обох. З цих причин порівняння ризику та користі наразі не доводить необхідність рутинного призначення селену жінкам з позитивними антитілами до ТПО під час вагітності. Крім того, пацієнти, які отримують селен, можуть мати підвищений ризик розвитку цукрового діабету 2 типу. Тож для впевненого декларування клінічного значення селену все ще потрібні додаткові клінічні докази.
- Selenium and thyroid diseases 2023 Mar 24:14:1133000.
- https://moz.gov.ua/
- Консенсусне керівництво з клінічної діагностики та лікування вузлів ЩЗ Американської асоціації клінічних ендокринологів (ААСЕ), Італійської асоціації клінічних ендокринологів (АМЕ), Європейської тиреоїдної асоціації (ЕТА), 2016.
- Guidelines for the Diagnosis and Management of Thyroid Disease during Pregnancy and the Postpartum (2017),
- Guidelines for Diagnosis and Management of Hyperthyroidism and other causes of Thyrotoxicosis (2016),
- Guidelines for the Treatment of Hypothyroidism (2014),
- 2022 ETA Guideline for the management of pediatric Graves’ disease,
- 2021 Evidence-Based Use of Levothyroxine/Liothyronine Combinations in Treating Hypothyroidism: A Consensus Document,
- 2018 ETA Guideline for the Management of Graves’ Hyperthyroidism,
- 2014 ETA Guidelines for the Management of Subclinical Hypothyroidism in Pregnancy and in Children,
- 2013 ETA Guideline: Management of Subclinical Hypothyroidism,
- 2012 ETA Guidelines: The Use of L-T4 + L-T3 in the Treatment of Hypothyroidism, Реверсивний Т3, 43rd Annual Meeting of the European Thyroid Association
- 2021, Clinical and laboratory aspects of 3,3’,5’-triiodothyronine (reverse T3), Does Reverse Triiodothyronine Testing Have Clinical Utility? An Analysis of Practice Variation Based on Order Data from a National Reference Laboratory
- Thyroid. 2018 Jul;28(7):842-848. Does Reverse Triiodothyronine Testing Have Clinical Utility? An Analysis of Practice Variation Based on Order Data from a National Reference Laborator,
- МОЗ Duodecim Medical Publications Ltd, >> 024.030 ebm00509 Обстеження пацієнта зі скаргами, що пов’язані зі щитоподібною залозою, >> 024.031 ebm00510 Вузлове або дифузне збільшення щитоподібної залози, >> 024.033 ebm00512 Аутоімунний тиреоїдит, >> 024.034 ebm00514 Гіпотиреоз, >> 024.035 ebm00513 Гіпертиреоз
- https://health-ua.com/
- Медична газета «Здоров’я України 21 сторіччя» № 15 (508), 2021 р.








