Для перегляду доступних досліджень та термінів їх виконання

Лабораторне обстеження онкогематологічного профілю
30.11.2021
З 15.05 2021 року медична лабораторія «Діла» актуалізує продуктовий портфель «Онкогематологія». Відтепер у Вас є можливість провести якісне, достовірне, точне і швидке лабораторне обстеження онгогематологічного профілю згідно із міжнародними стандартами. Дана стаття має оглядовий характер та має на меті розглянути деякі переваги та особливості цього обстеження.
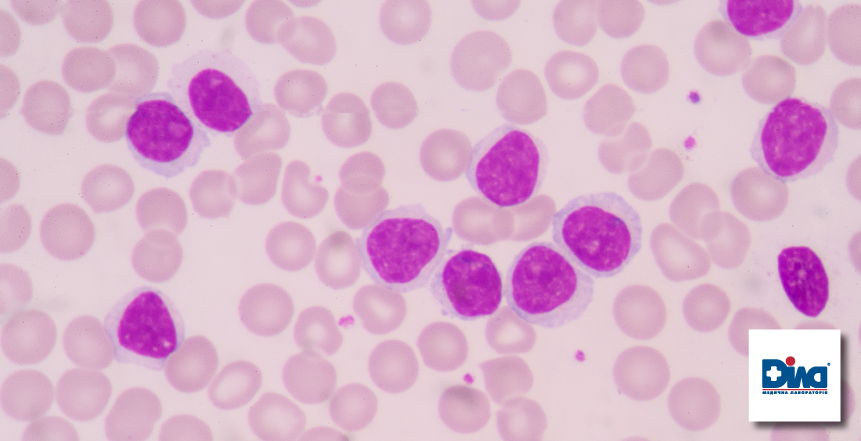
Встановлення діагнозу в онкогематологічній практиці спирається на спеціальну лабораторну діагностику – це поєднання методів морфології, імунофенотипування, цитохімії,молекулярних та цитогенетичних досліджень. Зазначені методи використовуються в певному об’ємі та в певній послідовності в залежності від клінічної ситуації. Морфологічне дослідження є базовим і необхідним, воно підтверджує присутність непластичних субстратних клітин в біологічному матеріалі. Якісно виконане морфологічне дослідження дає підґрунтя до наступних, більш складних і тривалих досліджень. Наприклад, якщо за даними мієлограми в кістковому мозку пухлинні клітини відсутні, то немає необхідності виконувати імунофенотипування, цитогенетичні або молекулярно-генетичні дослідження. Це дозволяє уникнути зайвих витрат, зусиль та зберегти час, що дуже важливо в умовах діагностики ургентних пацієнтів.
Тільки певна сходинко подібна послідовність та комплексність досліджень може забезпечити достовірну лабораторну діагностику онкогематологічних захворювань згідно із міжнародними стандартами NCCN, ESMО. Ми пропонуємо дослідження, що зручно поєднані в пакети або комплекси по 2 або більше досліджень. Цей перелік представлений в первинному направленні. Саме комплексність є особливістю продуктового портфелю «Онкогематологія» і вдало виділяє нашу лабораторію серед інших пропозицій.

В усьому світі лабораторна діагностика онкогематологічних захворювань – завдання підвищеної складності і потребує:
- Використання перевірених алгоритмів згідно із міжнародними стандартами
- Використання обладнання, що відповідає сучасним міжнародним стандартам
- Глибокого професійного досвіду лікаря вузького онкогематологічного профілю
Медична лабораторія «Діла» вдало поєднує всі ці вимоги.
I. Якщо лікар прагне встановити діагноз згідно із міжнародними стандартами, виникає необхідність у використанні стандартизованих, уніфікованих в усьому світі методик та алгоритмів. Медична лабораторія «Діла» отримала спеціалізований атестат про акредитацію виключно для медичних лабораторій – ДСТУ ISO 15189 і успішно працює згідно із цим стандартом.
В онкогематологічній практиці для використання стандартних нозологій МКХ-Онкологія (2016) поряд із стандартами в інших діагностичних напрямках, необхідно використовувати міжнародні алгоритми спеціальної лабораторної діагностики. Це можна яскраво проілюструвати на прикладі визначення імунофенотипу пухлини, що є одним з базових методів діагностики.
Імунофенотипування - це аналітичний процес встановлення типу і ступеню експресії клітинами окремих маркерів, т.з. CD - «кластерів диференціювання» (мембранних і внутрішньоклітинних), характерних для певної лінії кровотворення. Проточна цитофлюориметрія – метод імунофенотипування клітинних суспензій.
В нашій лабораторії підхід до імунофенотипування пухлинних клітин заснований на використанні стандартизованого покрокового алгоритму консорціуму EuroFlow, який був заснований у 2005 році і охоплює 20 дослідницьких груп з 11 країн світу. Метою є оновлення та стандартизація проточної цитометрії, що веде до глобального вдосконалення та прогресу в діагностиці онкогематологічних захворювань.

Згідно вказаного алгоритму імунофенотипування проводиться з використанням 10-12 -кольорових панелей антитіл, що дозволяє ідентифікувати і повністю охарактеризувати клонально розширені популяції патологічних клітин та зробити висновки про відповідність отриманого фенотипу певній патології згідно класифікації ВООЗ (остання версія WHO-O 2016 року). Особливого значення це набуває під час оцінки відповіді на лікування (т.з. Response Criteria) згідно із діючими міжнародними протоколами. Для моніторингу резистентного пулу пухлинних клітин (MRD) під час та після терапії застосовуються спеціалізовані високочутливі протоколи детекції малоклітинної популяції на тлі регенеруючого гемопоезу. Така проточна цитометрія називається NGF (Next Generation Flow). Чутливість метода складає мінімум 1 на 10 в 5 ступені ядровмісних клітин.
Дані протоколи дозволяють розмежувати нормальні клітини, що розвиваються (гематогони) та виявити залишкову популяцію клітин з пухлинним фенотипом. Як було вказано вище, імунофентипування методом проточної цитометрії запропоновано в комплексі з попереднім цитоморфологічним дослідженням.
II. Медична лабораторія «Діла» використовує новітнє обладнання від відомих виробників згідно міжнародних стандартів. Безпосередньо для виконання імунофенотипування пухлинних клітин згідно із алгоритмом консорціуму EuroFlow використовується прилад нового покоління BD FACSLyric, який поєднує в собі високу чутливість, простоту, швидкість, автоматизацію для полегшення робочого процесу та підвищення продуктивності. Оснащений 3 лазерами (синього, червоного, фіолетового), 12 каналами флуоресценції, 10 кольорами, прилад повністю відповідає високим вимогам консорціуму EuroFlow і забезпечує стандартизацію та співпрацю з будь-якими діагностичними центрами світу завдяки точним результатам та унікальним можливостям перенесення результатів аналізів.

III. Окрім дотримання високих міжнародних стандартів для якісної діагностики онкогематологічних захворювань потрібен глибокий професійний досвід лікаря вузької спеціалізації. В Україні і в цілому світі таких досвідчених професіоналів, які можуть точно і достовірно виконувати специфічні лабораторні дослідження - одиниці. Наші експерти – це команда визнаних професіоналів у діагностиці онкогематологічних захворювань, які регулярно відвідують курси підвищення кваліфікації українських та зарубіжних навчальних центрів, великих європейських лабораторій: Швеції, Іспанії, Франції.
Крім того, медична лабораторія «Діла» має статус клінічної бази кафедри клінічної імунології та алергології НМАПО ім. П. Л. Шупіка, приймає участь у міжнародних клінічних дослідженнях.
Молекулярні та цитогенетичні дослідження.
Особливої уваги слід приділити молекулярно-біологічним та цитогенетичним дослідженням під час діагностики онкогематологічних захворювань.
На сьогоднішній день провідне місце серед теорій лейкемогенезу займає молекулярно-генетична теорія, згідно з якою в основі злоякісної трансформації лежать структурно-функціональні зміни клітинних генів. Малігнізація нормальної клітини є результатом каскадного накопичення певних змін в генетичному матеріалі. Отже, злоякісна пухлина – це генетичне захворювання з фенотиповою та морфофункціональною гетерогенністю. Як згадувалось вище, у 2016 році класифікацію гематологічних новоутворень було переглянуто та доповнено з урахуванням знайдених унікальних біомаркерів, асоційованих з певними нозологічними формами. Зокрема, це стосується мутаційного статусу та рівня експресії генів. Тому особливої актуальності в лабораторній діагностиці злоякісних пухлин системи гемопоезу набуває виважене поєднання методів імунофенотипування, морфології, цитохімії з методами цитогенетики та молекулярної біології. Як правило, використовують FISH-аналіз з локус-специфічними ДНК-зондами та метод ПЛР (PCR), для більшої деталізації – каріотипування.
Інтенсивність експресії генів корелює з кількістю пухлинних клітин, що дозволяє визначати ступінь первинного пухлинного ураження і проводити моніторинг пухлинної маси для оцінки ефективності лікування. Характер мутацій обумовлює рівень ураження гемопоетичної клітини (рівень блокування її диференціювання), визначає морфоцитохімічні особливості та імунофенотип пухлинних клітин. Наявність тієї чи іншої аномалії каріотипу дозволяє судити про ступінь злоякісності пухлини і прогнозувати ефективність терапії. Ранжування хворих на онкогематологічні захворювання на групи сприятливого, проміжного і несприятливого характеристик прогнозу визначає тактику лікування. Виявлення певних молекулярно-генетичних маркерів пухлинних бластних клітин є першим кроком до таргетной терапії онкогематологічних захворювань та проведення диференційованого лікування в залежності від групи ризику. Прикладом успішної таргетной терапії гострого лейкозу є застосування препаратів трансретіноєвої кислоти при гострому промієлоцитарному лейкозі, інгібіторів тирозинкінази в поєднанні з поліхіміотерапією при Ph+ гострому мієлолейкозі та інше.
Генетичні маркери поряд з морфологічними, імунологічними, цитохімічними характеристиками пухлини, а також клінічними даними використовуються в якості критеріїв, що дозволяють виділити різні форми захворювань.
Зокрема, гострий лейкоз з t (12; 21) (p13; q22) TEL-AML1 (ETV6-RUNX1) - група сприятливого прогнозу. Частота повних ремісій сягає 90%, а безрецидивна 5-річна виживаність більше 80%. При гострому мієлолейкозі з t (8; 21) (q22; q22) в результаті транслокації відбувається злиття гена АМL1 на хромосомі 21 з геном ЕТО на хромосомі 8, утворюючи химерний ген АМL1-ЕТО на хромосомі 8. У процесі лікування рівень химерного гена зменшується на кілька порядків і відповідно збільшується перед рецидивом. При промієлоцитарному лейкозі у транслокацію залучені ген РМL, що кодує транскрипційний фактор на хромосомі 15 і RАRА-ген, який кодує альфа-рецептор ретиноєвої кислоти на хромосомі 17. Химерний білок PML/RARA обумовлює блок клітинного диференціювання і високу чутливість пухлинних клітин до ретиноєвої кислоти (ATRA). Наявність FLT3-ITD мутації у хворих на ГМЛ, у вигляді єдиної генетичної аберації або з іншими мутаціями, значно знижує показники безрецидивної і загальної виживаності. Навпаки, виявлення мутації в гені NPM1 або гені CEBPA при відсутності мутації FLT3-ITD асоціюється з більш сприятливим прогнозом. Перебудови гена JAK2 викликають негайну активацію JAK-STAT сигнального шляху. Патологічна передача сигналів JAK-STAT може бути нейтралізована за допомогою JAK-інгібіторів.
Комплексна оцінка прогностичних факторів, включаючи молекулярно-генетичні, дозволяє максимально точно стратифікувати групи ризику пацієнтів з гострим лейкозом і прогнозувати перебіг лейкемічного процесу, що може служити основою для оптимізації індивідуалізованого підходу до терапії з метою збільшення тривалості та поліпшення якості життя пацієнтів.
У випадку В-ХЛЛ, визначення делеції del 17р13 та/або мутації ТР53, мутаційного статусу генів IgHV дозволяє виділити групу пацієнтів (близько 10%), яким протипоказане лікування за стандартними схемами хіміо-імунотерапіі, тому що таке лікування сприяє збільшенню резистентності пухлини. Середня тривалість життя таких хворих у разі отримання стандартних схем не перевищує 11 місяців. Тому для хворих із делецією 17 хромосоми схемою вибору терапії першої лінії буде одна з таких без застосування хіміопрепаратів. При множинній мієломі, визначення t(4;14)(q13;q32), t(14;16) (MAF\IGH), del 1p32, del 17p13 дозволяє виділити групу хворих високого ризику, для яких показане застосування більш інтенсивного лікування вже на первинному етапі.
Своєчасна, комплексна та достовірна діагностика в онкогематології дозволяє прогнозувати перебіг захворювання та тривалість життя хворого, обрати адекватну тактику ведення хворого, тактику та схему лікування, визначити, чи є відповідь на лікування та глибину цієї відповіді.
Медична лабораторія «Діла» пропонує зручний та якісний інструмент, який дозволяє повною мірою використати можливості комплексної спеціальної лабораторної діагностики в онкогематологічній практиці. Стандатизація, автоматизація та профессіоналізм дозволять бути впевненими в достовірності отриманих результатах, а професіоналізм, відкритість і доброзичливість наших співробітників зробить процес обстеження максимально комфортним і перевершать всі Ваші сподівання.