Для перегляду доступних досліджень та термінів їх виконання

Глютен-залежні захворювання: особливості діагностики
16.03.2023
Останніми роками спостерігається підвищення інтересу до проблеми глютен-залежних захворювань. Глютен – основний білковий компонент пшениці, який виявляється і в інших зернових культурах, в тому числі у житі та ячмені. Патологія, яка ще недавно вважалася відносно рідкісною, стала нагадувати про себе все частіше і наполегливіше. У пшениці взагалі «не дуже добра слава» – незалежно від наявності целіакії чи інших патологій вона може бути причиною найрізноманітніших реакцій в організмі людини.
Станом на сьогодні, найбільш вивчені захворювання, пов’язані з глютеном – це
- алергія на білки пшениці, а саме:
- харчова
- респіраторна (астма пекаря)
- анафілаксія фізичного навантаження
- целіакія (глютенова ентеропатія)
- нова форма глютен-залежної патології – чутливість до глютену без целіакії (ЧГБЦ)
Актуальність глютен-залежних захворювань обумовлена:
- Надмірним споживанням глютеновмісних харчових продуктів та розвитком індустрії БГ ( безглютенових) продуктів
- Підвищеним вмістом глютену (клейковини) у сучасних сортах пшениці
- Призначенням некоректної діагностики (серологічної, генетичної, гістологічної, обстеження після призначення безглютенової дієти)
- Значною поширеністю ГЗ захворювань (целіакія 1-1,5%, ЧГБЦ 0,6-6%, алергія на пшеницю 0,4-4% населення)
- Недостатньою діагностикою (недостатня обізнаність лікарів, подібність симптомів з іншими захворюваннями)
Глютен-залежні захворювання мають багато спільного між собою:
- Поява симптомів після вживання в їжу глютену;
- Схожі гастроінтестінальні та деякі позакишкові симптоми;
- Зникнення симптомів при дотриманні БГД.
Всі три види глютензалежних реакцій відрізняються за клінічними, генетичними та гістологічними особливостями, що дозволяє провести диференційну діагностику. Скарги можуть бути дуже різноманітними, а кожна клінічна картина, з якою звертається до лікаря пацієнт – абсолютно унікальною. Перші прояви гастроінтестінальних симптомів: біль у животі, метеоризму, закрепу, блювоти - відрізняються по часу. При целіакії – це години, місяці, роки, при ЧГБЦ – години і дні, при алергії на пшеницю – хвилини та години.
Існує велика різноманітність позакишкових проявів ГЗЗ:

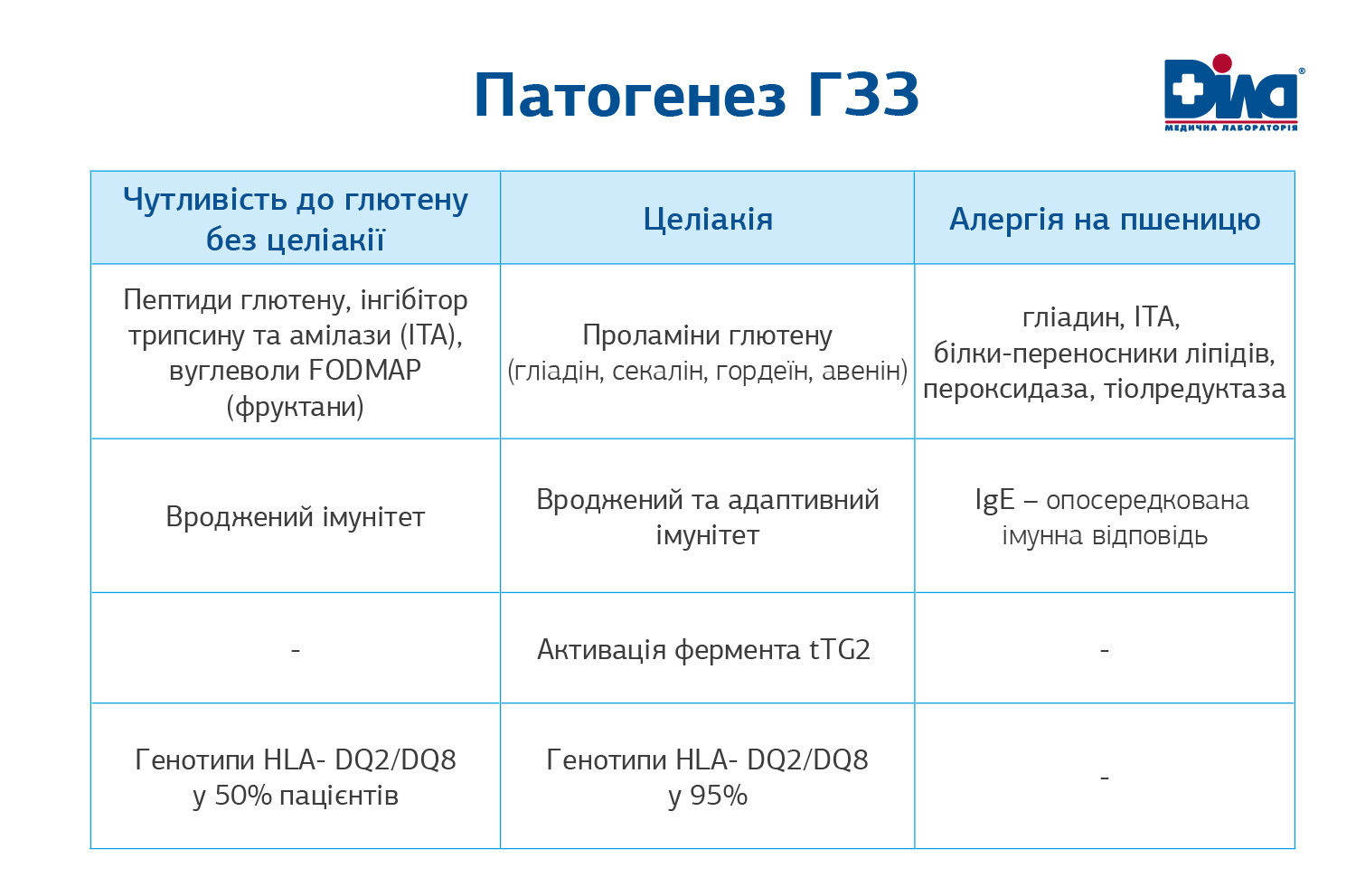
У чому ж різниця патогенезу ГЗЗ?
ЧГБЦ -захворювання, яке викликане білками глютену, вуглеводами FODMAPS в харчуванні, а також ІТА – інгібітором трипсину та амілази у пшениці.
Алергія на пшеницю - алергічна реакція на продукти, які містять пшеницю, реакція виникає при вживанні продуктів з їжею, тактильному контакті або вдиханні з повітрям.
Целіакія - аутоімунне захворювання, пов’язане з вживанням білків глютену. Основний патогенетичний механізм целіакії полягає у синтезі специфічних антитіл: до тканинної трансглутамінази, ендомізію, дезамінованих пептидів гліадину.
Головні фактори, що грають роль у патогенезі глютен-залежних захворювань:
1.Тригери: для ЧГБЦ - пептиди глютену, ITA – інгібітор трипсину та амілази, вуглеводи FODMAP (фруктани). ІTA можуть бути основними кандидатами-винуватцями тяжких форм глютенової (пшеничної) чутливості. Проламіни глютену – гліадін, секалін, гордеїн, авенін є тригерами для Целіакії. Білки переносники ліпідів, гліадін, пероксидаза, тіолредуктаза, ITA - для алергії на пшеницю. ITA – це рослинні білки, що пригнічують ферменти звичайних паразитів (борошняних черв’яків і клопів, що живуть у пшениці), а також відіграють важливу роль у метаболічних процесах, які відбуваються під час розвитку насіння і варіюються між сортів 2. Зміни в імунітеті: вроджений, адаптивний або IgE-опосредкована імунна відповідь. Наразі існує гіпотеза про те, що ITA можуть бути саме тими довгоочікуваними індукторами вродженого імунітету у пацієнтів з целіакією або ЧГБЦ. Важливо усвідомлювати кількість ITA – це 2-4% у загальному білку сучасної пшениці, а з глютеном ця частка складає вже 80-90%! 3. При целіакії відбувається активація ферменту тканинної трансглутамінази. Тканинна трансглутаміназа – це головна мішень антигенів при целіакії, що призводить до запуску Т-клітинного аутоімунного процесу 4. Щодо ролі генетичної діагностики: Особи, які є носіями генів HLA-DQ2 та/або HLA-DQ8, мають високий ризик розвитку патологічного стану, для нього характерна аномальна реакція організму на глютеновмісні продукти. Визначаються генотипи HLA- DQ2/DQ8 у 95% пацієнтів при целіакії та у 50% пацієнтів для ЧГБЦ.
Виявлення специфічних біомаркерів харчової алергії та скринінг целіакії - перший крок у діагностичному процесі.
Специфічні серологічні маркери цих захворювань:
|
|
ЧГБЦ | Целіакія | Алергія на пшеницю |
| Ig до тканинної трансглутамінази (TGA) | - | + | - |
| Ig до ендомізію (EMA) | - | + | - |
| Ig до дезамінованого гліадіну (DGP | - | + | - |
| Ig до гліадіну (AGA) | +/- | +/- | +/- |
| IgЕ до пептидів пшениці | - | - | + |
Al-Toma A, Volta U, Auricchio R, et al. European Society for the Study of Coeliac Disease (ESsCD) guideline for coeliac disease and other gluten-related disorders. United European Gastroenterol J. 2019;7(5):583-613. doi:10.1177/2050640619844125
Особливість дослідження Ig до гліадину (AGA) полягає в тому, що воно не є суто специфічним, і наразі не використовується в діагностиці Целіакії.
Гістохімічні зміни слизової оболонки кишківника при ГЗЗ можуть бути подібними між собою на початку захворювання - по класифікації (Марш 0-1).

Якщо ми маємо підозру на ГЗЗ. Першим кроком потрібно провести -Скринінг на целіакію, потім виключити алергію на пшеницю, а ЧГБЦ – залишається діагнозом виключення Діагностика є достовірною лише при попередньому щоденному (впродовж ≥6-ти тиж.) споживанні ≥1-ї страви, що містить глютен (≈10 г глютену на день — стільки містять 4 скибки хліба).
Алгоритм скринінгу целіакії: представлений у вигляді 2 кроків.

«Для початкової лабораторної діагностики рекомендують визначити рівні загального імуноглобуліну класу А (IgA) та IgA до тканинної трансглутамінази типу 2 (TGA-IgA), оскільки це є найбільш точним і економічно виправданим методом». European Society for Pediatric Gastroenterology, Hepatology and Nutrition; ESPGHAN 2020
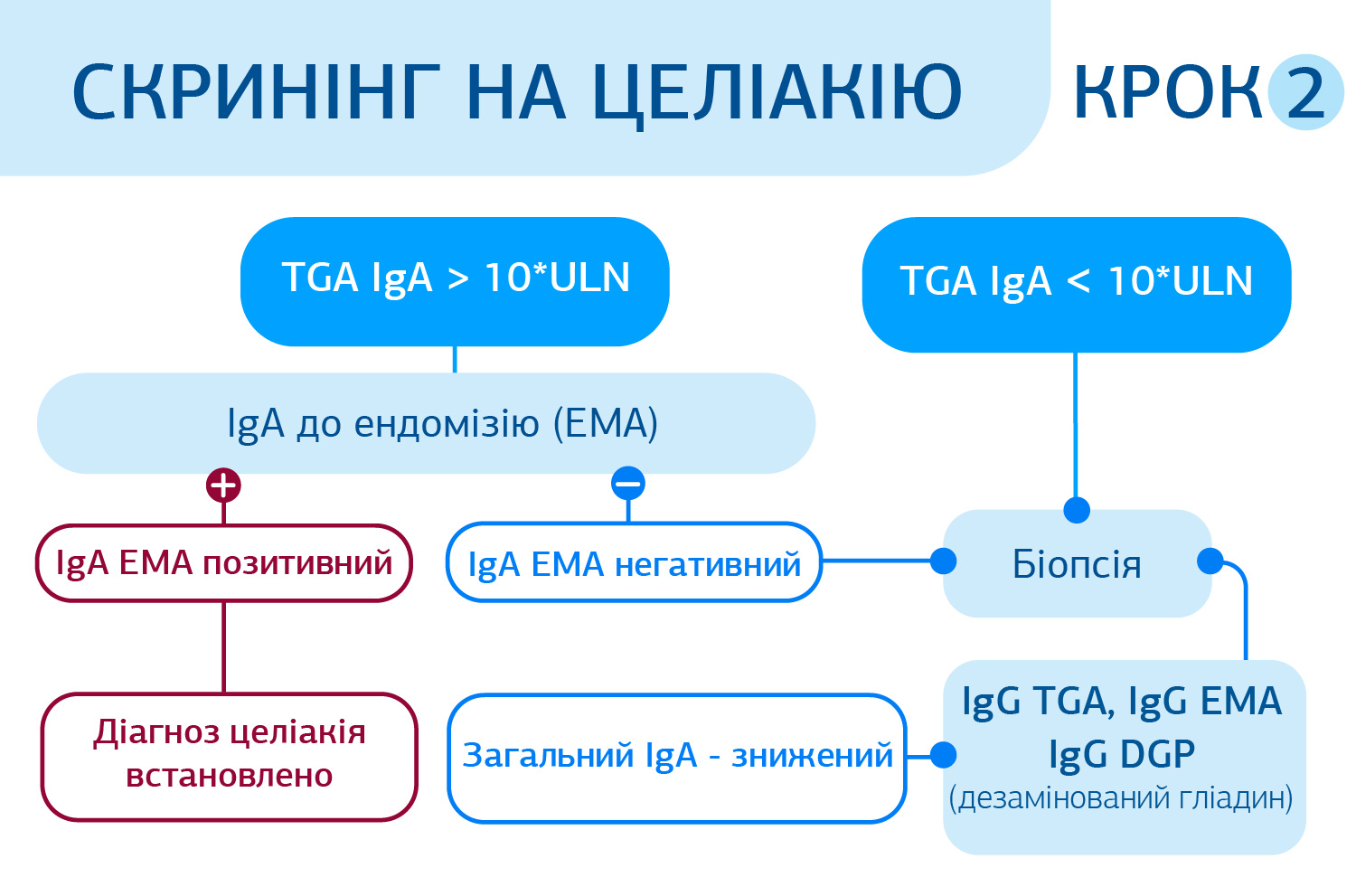
Згідно з оновленим Керівництвом Європейського товариства дитячих гастроентерологів, гепатологів і нутриціологів 2020 (European Society for Pediatric Gastroenterology, Hepatology and Nutrition; ESPGHAN), щодо діагностики целіакії в дітей та підлітків :
«Підтверджено, що діагноз целіакії може бути встановлений і без проведення біопсії в дітей з високим рівнем tTG -IgA (перевищує верхню межу норми ≥10 разів) та за наявності ендомізіальних антитіл (EMA-IgA) у другому зразку сироватки крові. Це міркування спрямоване на те, щоб уникнути неправильного маркування зразків або технічних помилок та підтвердити аутоімунітет целіакії за допомогою іншого тестового аналізу з високою специфічністю. IgA до ендомізію (IgA against endomysium) та IgG до дезамінованих пептидів гліадину (IgG against deamidated gliadin; DGP-IgG) не визначають на первинному етапі. У дітей з низьким рівнем загального IgA (низьким для відповідного віку або <0,2 г/л у дітей старше 3 років) як другий етап слід визначати IgG (DGP, EMA або tTG )».
Для діагностики целіакії МЛ «ДІЛА» рекомендує комплекс досліджень «Первинний скринінг целіакії» № 90, який з високою точністю дозволить виявити захворювання та розробити подальшу тактику ведення пацієнтів, адже:
- Склад комплексу відповідає міжнародним рекомендаціям по діагностиці глютензалежних захворювань.
- Діагностичні тести EliA™ Celikey® (IgG і IgA) мають високу специфічність та чутливість, це дозволяє в певних випадках уникнути процедури біопсії слизової кишківника.
- Працює алгоритм серологічної діагностики глютен-залежних захворювань на тестах другого покоління, які відповідають світовим і Європейським тенденціям діагностики.
- Дослідження виконуються на обладнанні світових виробників, а методики виконання відповідають регламентуючим документам.

Дослідження обов’язково слід пройти дітям, підліткам та дорослим у випадку:
1. Наявності симптомів при підозрі на целіакію;
2. При обтяженій спадковості (наявність целіакії у родичів 1 лінії) та наявності захворювань:
- цукровий діабет 1-го типу;
- синдром Дауна;
- аутоімунні захворювання печінки і/або щитоподібної залози;
- синдром Шерешевського-Тернера;
- синдром Вільямса- Бойрена;
- нефропатія IgА;
- дефіцит IgA.
3. Для диференційної діагностики у пацієнтів з алергією на пшеницю та гіперчутливістю до глютену, не спричиненою целіакією;
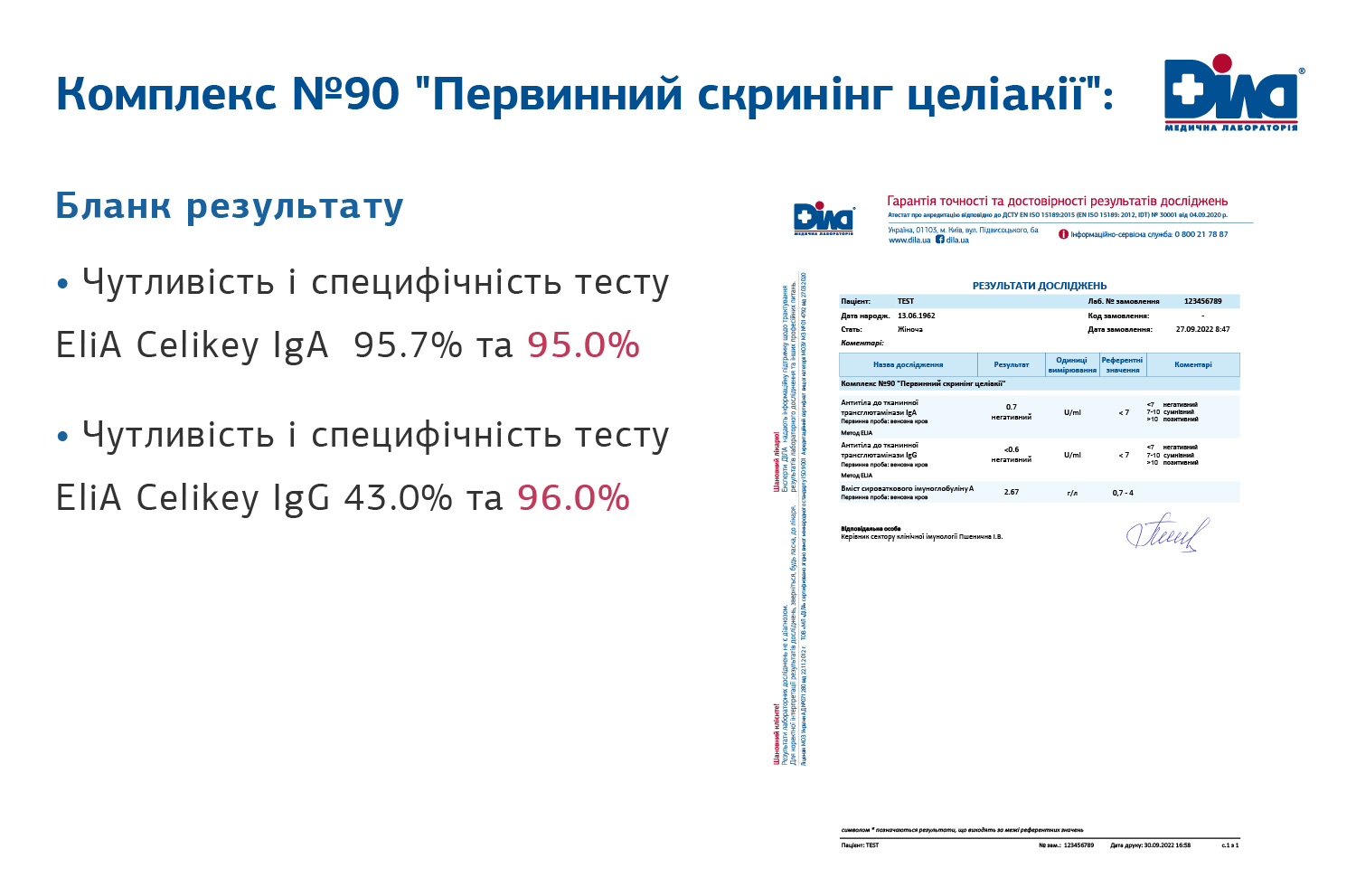
Згідно з рекомендаціями ESPGHAN у підході без біопсії повністю автоматизоване тестування за допомогою EliA Celikey IgA мінімізує кількість помилкових позитивних результатів, підвищуючи точність діагностики цього неінвазивного підходу.
Використана література:
- Al-Toma A, Volta U, Auricchio R, et al. European Society for the Study of Coeliac Disease (ESsCD) guideline for coeliac disease and other gluten-related disorders. United European Gastroenterol J. 2019;7(5):583-613. doi:10.1177/2050640619844125Niland B., Cash B.D. Health benefits and adverse effects of a gluten-free diet in non-celiac disease patients. Gastroenterol Hepatol (NY) 2018; 14: 82-91.
- Al-Toma A, Volta U, Auricchio R, et al. European Society for the Study of Coeliac Disease (ESsCD) guideline for coeliac disease and other gluten-related disorders. United European Gastroenterol J. 2019;7(5):583-613. doi:10.1177/2050640619844125
- Golley S., Corsini N., Topping D. et al. Motivations for avoiding wheat consumption in Australia: results from a population survey. Public Health Nutr 2015; 18: 490-499.
- ESPGHAN Guidelines for Diagnosing Coeliac Disease, 2019,2020
- Catassi C, Elli L, Bonaz B, et al. Diagnosis of Non-Celiac Gluten Sensitivity (NCGS): The Salerno Experts’ Criteria. Nutrients. 2015;7(6):4966-4977. doi:10.3390/nu7064966
- Sharma N, Bhatia S, Chunduri V, et al. Pathogenesis of Celiac Disease and Other Gluten Related Disorders in Wheat and Strategies for Mitigating Them. Front Nutr. 2020;7:6. Published 2020 Feb 7. doi:10.3389/fnut.2020.00006
- https://www.espghan.org/fileadmin/user_upload/IBD/ESPGHAN_Celiac_Guidelines_2019.pdf
- Lebwohl B., Sanders D.S., Green P.H.R. Coeliac disease. Lancet 2018; 391: 70-81.
- Catassi C., Alaedini A., Bojarski C. et al. The overlapping area of non-celiac gluten sensitivity (NCGS) and wheat-sensitive irritable bowel syndrome (IBS): an update. Nutrients 2017; 9:pii: E1268.
- Tanpowpong P., Ingham T.R., Lampshire P.K. et al. Coeliac disease and gluten avoidance in New Zealand children. Arch Dis Child 2012; 97: 12-16.
- Aziz I., Lewis N.R., Hadjivassiliou M. et al. A UK study assessing the population prevalence of self-reported gluten sensitivity and referral characteristics to secondary care. Eur J Gastroenterol Hepatol 2014; 26: 33-39.
- Carroccio A., Giambalvo O., Blasca F. et al. Self-reported non-celiac wheat sensitivity in high school students: demographic and clinical characteristics. Nutrients 2017; 9: pii: E771.
- Volta U., Tovoli F., Cicola R. et al. Serological tests in gluten sensitivity (nonceliac gluten intolerance). J Clin Gastroenterol 2012; 46: 680-685.
- Carroccio A., Mansueto P., Iacono G. et al. Nonceliac wheat sensitivity diagnosed by double-blind placebo-controlled challenge: exploring a new clinical entity. Am J Gastroenterol 2012; 107: 1898-1906.
- Lovell R.M., Ford A.C. Global prevalence of and risk factors for irritable bowel syndrome: a meta-analysis. Clin Gastroenterol Hepatol 2012; 10: 712-721.
- Carroccio A., Mansueto P., D’Alcamo A., Iacono G. Nonceliac wheat sensitivity as an allergic condition: personal experience and narrative review. Am J Gastroenterol 2013; 108: 1845-1852.
- Hollon J., Puppa E.L., Greenwald B. et al. Effect of gliadin on permeability of intestinal biopsy explants from celiac disease patients and patients with nonceliac gluten sensitivity. Nutrients 2015; 7: 1565-1576.
- Sapone A., Lammers K.M., Casolaro V. et al. Divergence of gut permeability and mucosal immune gene expression in two gluten-associated conditions: celiac disease and gluten sensitivity. BMC Med 2011; 9: 23.
- Portincasa P., Bonfrate L., de Bari O. et al. Irritable bowel syndrome and diet. Gastroenterol Rep (Oxf) 2017; 5: 11-19.
- Vazquez-Roque M.I., Camilleri M., Smyrk T. et al. A controlled trial of gluten-free diet in patients with irritable bowel syndrome-diarrhea: effects on bowel frequency and intestinal function. Gastroenterology 2013; 144: 903.e3-911.e3.
- Wu R.L., Vazquez-Roque M.I., Carlson P. et al. Gluten-induced symptoms in diarrhea-predominant irritable bowel syndrome are associated with increased myosin light chain kinase activity and claudin-15 expression. Lab Invest 2017; 97: 14-23.
- Fritscher-Ravens A., Schuppan D., Ellrichmann M. et al. Confocal endomicroscopy shows food-associated changes in the intestinal mucosa of patients with irritable bowel syndrome. Gastroenterology 2014; 147: 1012.e4-1020.e4.
- Schuppan D., Zevallos V. Wheat amylase trypsin inhibitors as nutritional activators of innate immunity. Dig Dis 2015; 33: 260-263.
- Reig-Otero Y., Manes J., Manyes L. Amylase-trypsin inhibitors in wheat and other cereals as potential activators of the effects of nonceliac gluten sensitivity. J Med Food 2018; 21: 207-214.
- Gomez L., Martin E, Hernandez D. et al. Members of the alpha-amylase inhibitors family from wheat endosperm are major allergens associated with baker’s asthma. FEBS Lett 1990; 261: 85-88.
- Junker Y., Zeissig S., Kim S.J. et al. Wheat amylase trypsin inhibitors drive intestinal inflammation via activation of toll-like receptor 4. J Exp Med 2012; 209: 2395-2408.
- de Punder K., Pruimboom L. The dietary intake of wheat and other cereal grains and their role in inflammation. Nutrients 2013; 5: 771-787.
- Murray K., Wilkinson-Smith V., Hoad C. et al. Differential effects of FODMAPs (fermentable oligo-, di-, mono-saccharides and polyols) on small and large intestinal contents in healthy subjects shown by MRI. Am J Gastroenterol 2014; 109: 110-119.
- Spiller R. How do FODMAPs work? J Gastroenterol Hepatol 2017; 32 Suppl 1: 36-39.
- Catassi C., Elli L., Bonaz B. et al. Diagnosis of non-celiac gluten sensitivity (NCGS): the Salerno Experts’ Criteria. Nutrients 2015; 7: 4966-4977.
- https://www.vz.kiev.ua/neperenosymist-glyutenu-bez-tseliakiyi-yak-diagnostuvaty-i-likuvaty/ Непереносимість глютену без целіакії: як діагностувати і лікувати?
- ГЛЮТЕН-ЧУТЛИВА ЕНТЕРОПАТІЯ: СТАН ПРОБЛЕМИ НА СУЧАСНОМУ ЕТАПІ. Горобець А.О Національний медичний університет імені О.О. Богомольця, м. Київ,
- https://health-ua.com/article/41194-oberezhnoglyuten--sho-neobhdno-znati-pro-tcelakyu








