Для перегляду доступних досліджень та термінів їх виконання

Харчова алергія у XXI столітті: сучасні підходи до діагностики, стратифікації ризику та клінічного менеджменту
07.04.2021Професор Олена Шарікадзе
Вступ
Харчова алергія визначається як імунологічно опосередкована патологічна реакція на харчові продукти, яка виникає при повторному контакті з алергеном та супроводжується клінічними симптомами різного ступеня тяжкості. Цей стан є однією з найбільш актуальних проблем клінічної алергології 21 століття. За останні десятиліття відзначається значне зростання поширеності алергічних захворювань, що пов’язано зі змінами харчування, впливом факторів довкілля та особливостями імунної відповіді. Водночас харчова алергія характеризується високим рівнем гіпердіагностики та значною варіабельністю клінічних проявів. Сучасні рекомендації міжнародних професійних товариств (EAACI, GA²LEN) підкреслюють важливість клінічного анамнезу, доказових методів діагностики та використання молекулярної алергодіагностики для уточнення механізмів сенсибілізації.
Окрему увагу привертає проблема стратифікації ризику тяжких реакцій, зокрема анафілаксії. Перспективним біомаркером у цьому контексті є базальний рівень сироваткової триптази, який може відображати функціональний стан опасистих клітин та асоціюватися з підвищеним ризиком тяжких реакцій при харчовій алергії.
Важливо розрізняти поняття сенсибілізації та клінічно значущої алергії, оскільки наявність специфічних IgE не завжди супроводжується клінічними проявами.
Харчова алергія належить до патологій із найбільшою частотою хибної діагностики, що часто призводить до необґрунтованих елімінаційних дієт та погіршення якості життя пацієнтів.
Поширеність харчової алергії
За даними міжнародних досліджень, поширеність харчової алергії становить:
- 2–4 % серед дітей та дорослих;
- до 6 % серед дітей віком до 17 років;
- до 10 % на першому році життя.
Найчастішими алергенами у дітей раннього віку є:
- білки коров’ячого молока;
- яйця;
- пшениця;
- соя.
- У старшому віці зростає значення:
- горіхів;
- арахісу;
- риби та морепродуктів.
При цьому лише невелика частка випадків харчової гіперчутливості підтверджується провокаційними тестами.
Реакції на їжу поділяють на імунні та неімунні. Серед імунних найбільш важливими є IgE-опосередковані реакції, які мають найбільший вплив на стан здоров’я людини. IgE-опосередковані реакції на їжу займають перше місце серед причин розвитку анафілаксії та анафілактичного шоку. Класифікація реакцій гіперчутливості на їжу та базові клінічні симптоми представлені в таблиці 1.
У той же час переважна більшість реакцій на їжу залежить від неімунних механізмів (непереносимість лактози, реакції на біогенні аміни. токсичні реакції), проте, також може бути причиною розвитку рідкісної неімунної форми анафілаксії. Такий спектр патологій обумовлює складність диференційної діагностики.
Таблиця 1.
Основні типи реакцій харчової гіперчутливості
| Тип реакції: IgE-опосередкована харчова алергія | |
| Механізм | IgE-медіаторна активація опасистих клітин |
| Приклади захворювань | Кропив’янка, анафілаксія, оральний алергічний синдром |
| Час появи симптомів | Хвилини – 2 години |
| Основні прояви | Кропив’янка, ангіоедема, бронхоспазм, анафілаксія |
| Тип реакції: Не-IgE-опосередкована алергія | |
| Механізм | Клітинно-опосередкована імунна реакція |
| Приклади захворювань | FPIES, харчова ентеропатія |
| Час появи симптомів | Години – дні |
| Основні прояви | Блювання, діарея, мальабсорбція |
| Тип реакції: Змішаний механізм | |
| Механізм | IgE + клітинний імунітет |
| Приклади захворювань | Еозинофільний езофагіт |
| Час появи симптомів | Хронічний перебіг |
| Основні прояви | Дисфагія, біль у животі |
| Тип реакції: Неімунні реакції | |
| Механізм | Ферментативні або фармакологічні механізми |
| Приклади захворювань | Непереносимість лактози, гістамінова інтолерантність |
| Час появи симптомів | Варіабельно |
| Основні прояви | Метеоризм, діарея, головний біль |
Основним етіологічним чинником розвитку IgE-опосередкованої харчової алергії є певні продукти з високим імуногенним потенціалом, які здатні викликати реакції, що відповідальні за розвиток різноманітних клінічних симптомів у пацієнтів. Найпоширеніші харчові алергени та головні молекули у складі даних алергенів представлені у таблиці 2.
Таблиця 2.
Найпоширеніші харчові алергени у дітей та дорослих
| Алерген | Основні алергенні білки | Особливості реакцій |
| Коров’яче молоко | Bos d 4, Bos d 5, Bos d 8 | Частіше у дітей раннього віку |
| Яйце | Gal d 1, Gal d 2 | Може зникати з віком |
| Арахіс | Ara h 1, Ara h 2, Ara h 3 | Високий ризик анафілаксії |
| Горіхи | Cor a 9, Jug r 1 | Стійка сенсибілізація |
| Риба | Парвальбуміни | Часті системні реакції |
| Морепродукти | Тропоміозин | Перехресна реактивність з кліщами |
| Пшениця | ω-5-гліадин | Може бути пов’язана з анафілаксією, індукованою фізичним навантаженням |
Разом із глобалізацією світу та розширенням можливості транспортування різних видів продуктів у різні країни з’являються нові виклики у вигляді розширення спектру харчових алергенів.
У якості прикладів рідкісних та нових харчових алергенів можна відмітити наступні:
- їстівні комахи;
- люпин;
- екзотичні види м’яса;
- спеції та добавки.
Варто пам’ятати, що перехресна реактивність відіграє важливу роль у розвитку таких реакцій. Наприклад:
- тропоміозин є спільним алергеном у ракоподібних та комах;
- люпин має перехресну реактивність з арахісом.
Актуальність проблеми харчової алергії безпосередньо детермінована ризиком розвитку анафілаксії як її найбільш тяжкої клінічної форми. Анафілаксія ‒ системна реакція гіперчутливості, що зазвичай розвивається швидко та може становити безпосередню загрозу для життя. Сучасні рекомендації (EAACI, 2021; AAAAI/ACAAI, 2023; GA2LEN, 2024) підкреслюють, що анафілаксія є насамперед клінічним діагнозом, який встановлюється на підставі поєднання анамнезу, характеру симптомів, часу їх виникнення, можливого тригера, наявності кофакторів та відповіді на лікування. Водночас рішення про введення епінефрину не потребує формального підтвердження діагностичних критеріїв анафілаксії, а позитивна клінічна відповідь на епінефрин не може розглядатися як сурогатний маркер діагнозу.
Визначення триптази набуває дедалі більшого значення у сучасному алгоритмі ведення пацієнтів із харчовою анафілаксією. Підвищення гострої сироваткової триптази підтримує діагноз анафілаксії, однак нормальний показник не виключає системної активації опасистих клітин. У клінічній практиці особливу цінність має порівняння гострого рівня із базальним: підвищення гострої триптази щонайменше на 20% + 2 нг/мл від базального рівня розглядається як доказ системної мастоцитарної активації. Базальний рівень триптази доцільно визначати в осіб із рецидивною, ідіопатичною або тяжкою анафілаксією, а також за наявності підозри на мастоцитоз чи інші клональні мастоцитарні розлади. Якщо базовий рівень становить ≥8 нг/мл, слід розглядати подальшу оцінку щодо спадкової альфа-триптаземії.
Дані українського позиційного документа додатково підтримують використання базальної триптази саме як інструмента стратифікації ризику тяжких анафілактичних реакцій при харчовій алергії. Для пацієнтів із підвищеним базового рівня триптази рекомендовані інтенсивніше навчання, профілактичні заходи та більш індивідуалізований підхід до ведення. При оцінці ризику анафілаксії особливої уваги потребують діти раннього віку. Дана вікова група має низку діагностичних особливостей:
- маленькі діти не здатні чітко вербалізувати симптоми;
- деякі ознаки можуть маскуватися під звичну поведінку або інші стани.
Через відсутність окремих валідованих критеріїв для цієї вікової категорії рекомендовано застосовувати чинні критерії NIAID/FAAN або AAFA’s (малюнок 1). Важливо, що вік дитини не корелює з тяжкістю реакції, а анафілаксія рідко є першою маніфестацією при першому введенні харчового алергену; значно частіше дебютують легші, переважно шкірні реакції.
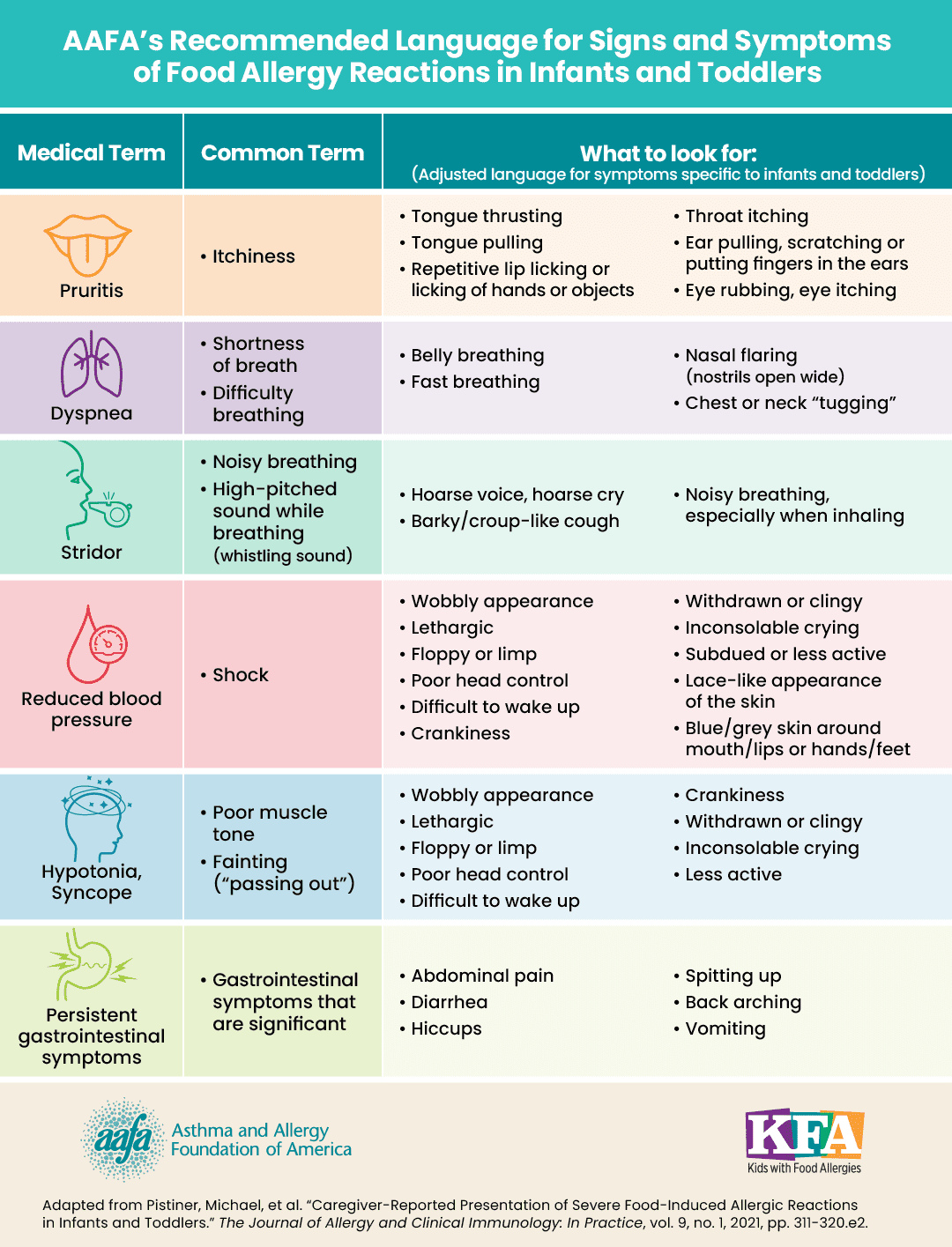
Малюнок 1. Ознаки анафілаксії у дітей раннього віку.
Матеріал із сайту https://aafa.org/asthma-allergy-research/our-research/food-allergy-anaphylaxis-in-infants/
Діагностика різних форм харчової алергії залишається складною проблемою, міжнародні рекомендації зазначають, що єдиним «золотим діагностичним стандартом» при будь якій формі харчовій алергії залишається провокаційний оральний тест (сліпий або відкритий). Проте його проведення має великі ризики, особливо якщо мова йде про тяжкі реакції та анафілаксію. Тому останнім часом все частіше використовується компонентна діагностика, яка допомагає визначити сенсибілізацію до алергенних молекул їжі.
Нижче наводимо діагностичний алгоритм, запропонований EAACI:
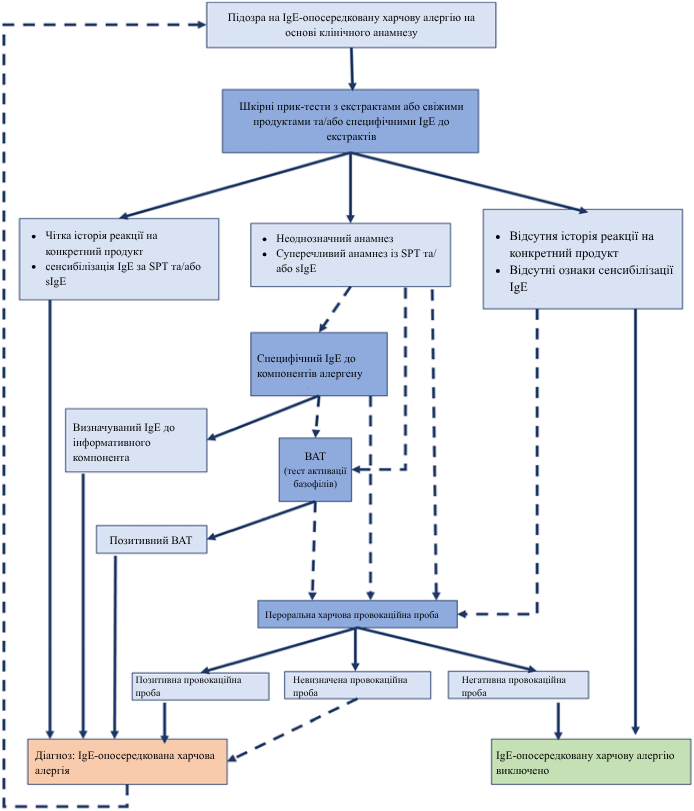
Малюнок 2 Алгоритм діагностики IgE-опосередкованої харчової алергії
Оригінал - https://onlinelibrary.wiley.com/doi/10.1111/all.15902
Згідно рекомендацій EAACI тестами першої лінії є специфічні IgE до екстракту алергену або ШПТ, а молекулярна діагностика є тестами другої лінії. EAACI не рекомендує використовувати широкі панелі чи мультиплексні дослідження як тести першої лінії через високу частоту виявлення латентної сенсибілізації.
Одним з перспективних та ефективних напрямків діагностики є компонентна (молекулярна) діагностика, що дозволяє визначити конкретні молекули-алергени, зазвичай представлені специфічними білками.
Це має важливе значення для:
- прогнозування тяжкості реакцій;
- оцінки перехресної реактивності;
- вибору тактики лікування.
Використання монокомпонентних та багатокомпонентних платформ значно покращує можливості діагностики при підозрі на харчову алергію.
Біомаркери тяжкості харчової алергії (таблиця 3).
Прогнозування ризику анафілаксії залишається важливою проблемою клінічної алергології. Перспективним маркером є базальний рівень сироваткової триптази. Дослідження показали, що підвищений рівень триптази може бути асоційований з більш високим ризиком тяжких анафілактичних реакцій. Згідно з сучасними даними, значення ≥8 мкг/л можуть бути пов’язані з підвищеною ймовірністю тяжких реакцій.
Важливо, що визначення триптази рекомендується розглядати як інструмент стратифікації ризику, а не як діагностичний тест алергії.
Таблиця 3.
Біомаркери тяжкості харчової алергії
| Біомаркер | Клінічне значення |
| Специфічні IgE | Підтвердження сенсибілізації |
| Компонентна алергодіагностика | Прогноз тяжкості реакції |
| Базальний рівень сироваткової триптази | Оцінка ризику тяжкої анафілаксії |
| БАТ (тест активації базофілів) | Функціональна оцінка реактивності |
Менеджмент пацієнтів з харчовою алергією
Для пацієнтів із підтвердженою харчовою алергією ключовим компонентом менеджменту є цілеспрямована освіта щодо уникнення алергену, раннього розпізнавання симптомів та правильного використання епінефрину. Отже, практичне консультування повинно концентруватися передусім на запобіганні ненавмисному вживанню, контролі прихованих алергенів, безпеці харчування поза домом, у подорожах, школі та закладах громадського харчування.
Епінефрин залишається препаратом першої лінії при анафілаксії. Наявні дані свідчать, що його раннє введення асоційоване з кращими клінічними результатами, нижчим ризиком біфазної реакції та меншою потребою в госпіталізації. Затримка введення епінефрину описується серед факторів несприятливого перебігу, а у серіях летальних випадків лікування нерідко було несвоєчасним. Водночас превентивне використання епінефрину у безсимптомного пацієнта після ймовірного контакту з алергеном не має достатньої доказової підтримки та не повинно розглядатися як рутинна тактика. Індивідуалізований підхід до пацієнта є ключовим для підвищення безпеки лікування.
Висновки
- Харчова алергія є складною мультифакторною патологією із значною клінічною варіабельністю.
- Ключовим елементом діагностики залишається детальний клінічний анамнез.
- Молекулярна алергологія відкриває нові можливості для персоналізованої діагностики та прогнозування ризику реакцій.
- Базальний рівень триптази може використовуватися як біомаркер стратифікації ризику тяжких анафілактичних реакцій.
- Подальші дослідження необхідні для вдосконалення алгоритмів діагностики та лікування харчової алергії.
Література
- Muraro A, Worm M, et all European Academy of Allergy and Clinical Immunology, Food Allergy, Anaphylaxis Guidelines Group. EAACI guidelines: Anaphylaxis (2021 update). Allergy. 2022 Feb;77(2):357-377. doi: 10.1111/all.15032.
- EAACI guidelines on the diagnosis of IgE-mediated food allergy Alexandra F. Santos, Carmen Riggioni, Ioana Agache, at all Allergy, 2023, 78(12) https://doi.org/10.1111/all.15902
- Managing food allergy: GA2LEN guideline 2022 GA2LEN Food Allergy Guideline Group et al. World Allergy Organization Journal, Volume 15, Issue 9, 100687
- Anaphylaxis: A 2023 practice parameter update CollaboratorsWorkgroup ContributorsJoint Task Force on Practice Parameters Reviewers et al. Annals of Allergy, Asthma & Immunology, Volume 132, Issue 2, 124 – 176.
- Loli-Ausejo D, Gonzalez-Matamala MF, Martí D, Ruano-Zaragoza M, Mir-Ihara P, Solis-Ynga K, Lara R, Bartra J, Pascal M, Muñoz-Cano R. Basal Serum Tryptase Outperforms Hereditary Alpha Tryptasemia as a Biomarker of Food Allergy Severity. Allergy. 2025 Aug;80(8):2376-2378. doi: 10.1111/all.16623.
- Tedner SG, Asarnoj A, et all Food allergy and hypersensitivity reactions in children and adults-A review. J Intern Med. 2022 Mar;291(3):283-302. doi: 10.1111/joim.13422.
- Loprinzi Brauer CE, Motosue MS, Li JT, Hagan JB, Bellolio MF, Lee S, Campbell RL. Prospective Validation of the NIAID/FAAN Criteria for Emergency Department Diagnosis of Anaphylaxis. J Allergy Clin Immunol Pract. 2016 Nov-Dec;4(6):1220-1226. doi: 10.1016/j.jaip.2016.06.003.








