
ПИЩЕВАЯ АЛЛЕРГИЯ В XXI ВЕКЕ: СОВРЕМЕННЫЕ ПОДХОДЫ К ДИАГНОСТИКЕ, СТРАТИФИКАЦИИ РИСКА И КЛИНИЧЕСКОМУ ВЕДЕНИЮ
07.04.2021Профессор Елена Шарикадзе
Введение
Пищевая аллергия определяется как иммунологически опосредованная патологическая реакция на пищевые продукты, которая возникает при повторном контакте с аллергеном и сопровождается клиническими симптомами различной степени тяжести. Это состояние является одной из наиболее актуальных проблем клинической аллергологии XXI века. За последние десятилетия отмечается значительный рост распространенности аллергических заболеваний, что связано с изменениями в питании, влиянием факторов окружающей среды и особенностями иммунного ответа. В то же время пищевая аллергия характеризуется высоким уровнем гипердиагностики и значительной вариабельностью клинических проявлений. Современные рекомендации международных профессиональных обществ (EAACI, GA²LEN) подчеркивают важность клинического анамнеза, доказательных методов диагностики и использования молекулярной аллергодиагностики для уточнения механизмов сенсибилизации.
Особое внимание привлекает проблема стратификации риска тяжелых реакций, в частности анафилаксии. Перспективным биомаркером в этом контексте является базальный уровень сывороточной триптазы, который может отражать функциональное состояние тучных клеток и ассоциироваться с повышенным риском тяжелых реакций при пищевой аллергии.
Важно различать понятия сенсибилизации и клинически значимой аллергии, поскольку наличие специфических IgE не всегда сопровождается клиническими проявлениями.
Пищевая аллергия относится к патологиям с наибольшей частотой ложной диагностики, что часто приводит к необоснованным элиминационным диетам и ухудшению качества жизни пациентов.
Распространенность пищевой аллергии
По данным международных исследований, распространенность пищевой аллергии составляет:
- 2–4 % среди детей и взрослых;
- до 6 % среди детей в возрасте до 17 лет;
- до 10 % на первом году жизни.
Наиболее частыми аллергенами у детей раннего возраста являются:
- белки коровьего молока;
- яйца;
- пшеница;
- соя.
- В старшем возрасте возрастает значение:
- орехов;
- арахиса;
- рыбы и морепродуктов.
При этом лишь небольшая доля случаев пищевой гиперчувствительности подтверждается провокационными тестами.
Реакции на пищу делят на иммунные и неиммунные. Среди иммунных наиболее важными являются IgE-опосредованные реакции, которые оказывают наибольшее влияние на состояние здоровья человека. IgE-опосредованные реакции на пищу занимают первое место среди причин развития анафилаксии и анафилактического шока. Классификация реакций гиперчувствительности на пищу и базовые клинические симптомы представлены в таблице 1.
В то же время подавляющее большинство реакций на пищу обусловлено неиммунными механизмами (непереносимость лактозы, реакции на биогенные амины, токсические реакции), однако они также могут быть причиной развития редкой неиммунной формы анафилаксии. Такой спектр патологий обусловливает сложность дифференциальной диагностики.
Таблица 1.
Основные типы реакций пищевой гиперчувствительности
| Тип реакции: IgE-опосредованная пищевая аллергия | |
| Механизм | IgE-опосредованная активация тучных клеток |
| Примеры заболеваний | Крапивница, анафилаксия, оральный аллергический синдром |
| Время появления симптомов | Минуты – 2 часа |
| Основные проявления | Крапивница, ангиоотек, бронхоспазм, анафилаксия |
| Тип реакции: Не-IgE-опосредованная аллергия | |
| Механизм | Клеточно-опосредованная иммунная реакция |
| Примеры заболеваний | FPIES, пищевая энтеропатия |
| Время появления симптомов | Часы – дни |
| Основные проявления | Рвота, диарея, мальабсорбция |
| Тип реакции: Смешанный механизм | |
| Механизм | IgE + клеточный иммунитет |
| Примеры заболеваний | Эозинофильный эзофагит |
| Время появления симптомов | Хроническое течение |
| Основные проявления | Дисфагия, боль в животе |
| Тип реакции: Неиммунные реакции | |
| Механизм | Ферментативные или фармакологические механизмы |
| Примеры заболеваний | Непереносимость лактозы, гистаминовая непереносимость |
| Время появления симптомов | Вариабельно |
| Основные проявления | Метеоризм, диарея, головная боль |
Основным этиологическим фактором развития IgE-опосредованной пищевой аллергии являются определенные продукты с высоким иммуногенным потенциалом, которые способны вызывать реакции, ответственные за развитие разнообразных клинических симптомов у пациентов. Наиболее распространенные пищевые аллергены и главные молекулы в составе данных аллергенов представлены в таблице 2.
Таблица 2.
Наиболее распространенные пищевые аллергены у детей и взрослых
| Аллерген | Основные аллергенные белки | Особенности реакций |
| Коровье молоко | Bos d 4, Bos d 5, Bos d 8 | Чаще у детей раннего возраста |
| Яйцо | Gal d 1, Gal d 2 | Может исчезать с возрастом |
| Арахис | Ara h 1, Ara h 2, Ara h 3 | Высокий риск анафилаксии |
| Орехи | Cor a 9, Jug r 1 | Стойкая сенсибилизация |
| Рыба | Парвальбумины | Частые системные реакции |
| Морепродукты | Тропомиозин | Перекрестная реактивность с клещами |
| Пшеница | ω-5-глиадин | Может быть связана с анафилаксией, индуцированной физической нагрузкой |
Вместе с глобализацией мира и расширением возможности транспортировки различных видов продуктов в разные страны появляются новые вызовы в виде расширения спектра пищевых аллергенов.
В качестве примеров редких и новых пищевых аллергенов можно отметить следующие:
- съедобные насекомые;
- люпин;
- экзотические виды мяса;
- специи и добавки.
Стоит помнить, что перекрестная реактивность играет важную роль в развитии таких реакций. Например:
- тропомиозин является общим аллергеном у ракообразных и насекомых;
- люпин имеет перекрестную реактивность с арахисом.
Актуальность проблемы пищевой аллергии непосредственно детерминирована риском развития анафилаксии как ее наиболее тяжелой клинической формы. Анафилаксия ‒ системная реакция гиперчувствительности, которая обычно развивается быстро и может представлять непосредственную угрозу для жизни. Современные рекомендации (EAACI, 2021; AAAAI/ACAAI, 2023; GA2LEN, 2024) подчеркивают, что анафилаксия является прежде всего клиническим диагнозом, который устанавливается на основании сочетания анамнеза, характера симптомов, времени их возникновения, возможного триггера, наличия кофакторов и ответа на лечение. В то же время решение о введении эпинефрина не требует формального подтверждения диагностических критериев анафилаксии, а положительный клинический ответ на эпинефрин не может рассматриваться как суррогатный маркер диагноза.
Определение триптазы приобретает все большее значение в современном алгоритме ведения пациентов с пищевой анафилаксией. Повышение острой сывороточной триптазы поддерживает диагноз анафилаксии, однако нормальный показатель не исключает системной активации тучных клеток. В клинической практике особую ценность имеет сравнение острого уровня с базальным: повышение острой триптазы по крайней мере на 20% + 2 нг/мл от базального уровня рассматривается как доказательство системной мастоцитарной активации. Базальный уровень триптазы целесообразно определять у лиц с рецидивирующей, идиопатической или тяжелой анафилаксией, а также при наличии подозрения на мастоцитоз или другие клональные мастоцитарные расстройства. Если базовый уровень составляет ≥8 нг/мл, следует рассматривать дальнейшую оценку на предмет наследственной альфа-триптаземии.
Данные украинского позиционного документа дополнительно поддерживают использование базальной триптазы именно как инструмента стратификации риска тяжелых анафилактических реакций при пищевой аллергии. Для пациентов с повышенным базальным уровнем триптазы рекомендуются более интенсивное обучение, профилактические меры и более индивидуализированный подход к ведению. При оценке риска анафилаксии особого внимания требуют дети раннего возраста. Данная возрастная группа имеет ряд диагностических особенностей:
- маленькие дети не способны четко вербализовать симптомы;
- некоторые признаки могут маскироваться под привычное поведение или другие состояния.
Из-за отсутствия отдельных валидированных критериев для этой возрастной категории рекомендовано применять действующие критерии NIAID/FAAN или AAFA's (рисунок 1). Важно, что возраст ребенка не коррелирует с тяжестью реакции, а анафилаксия редко является первой манифестацией при первом введении пищевого аллергена; значительно чаще дебютируют более легкие, преимущественно кожные реакции.
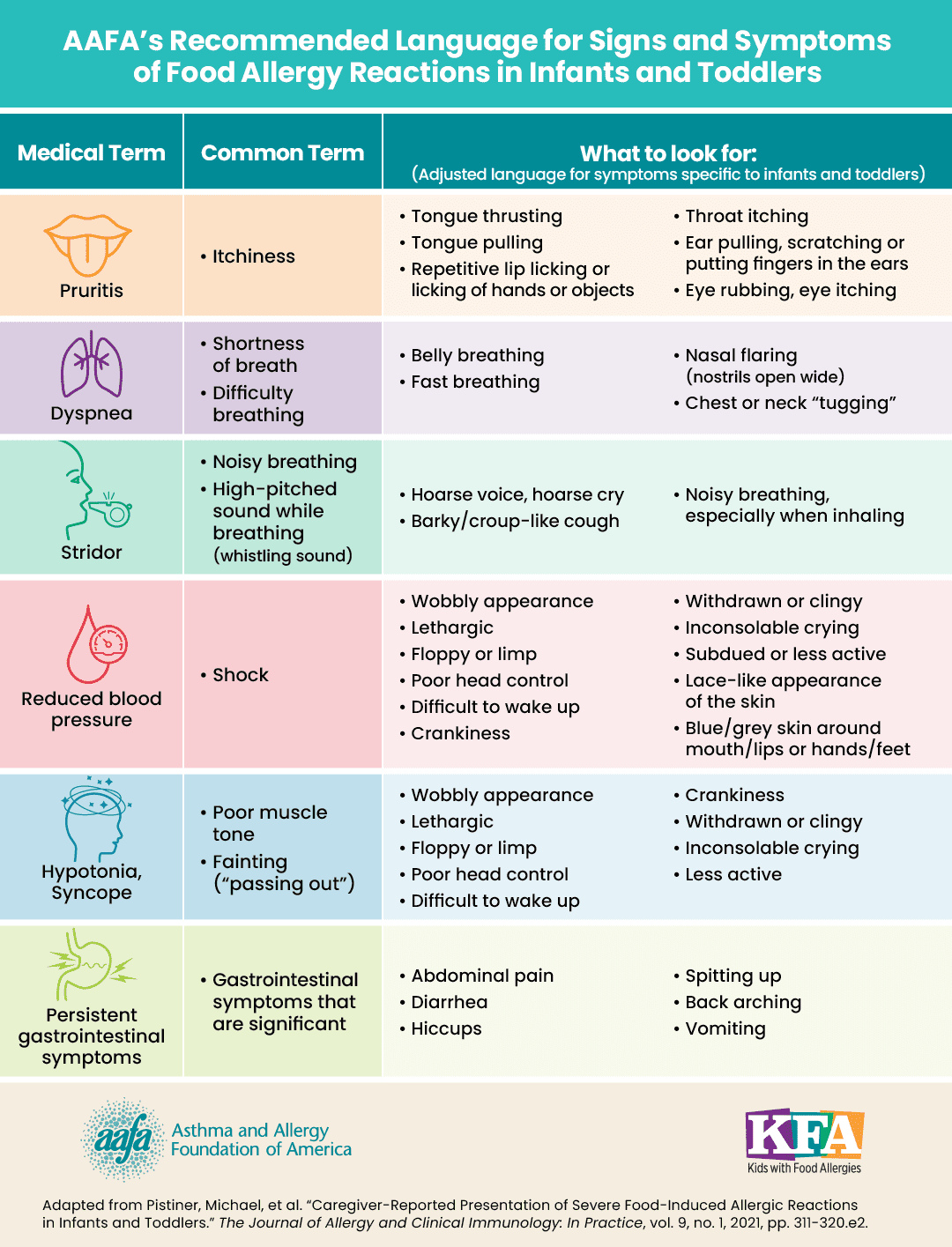
Рисунок 1. Признаки анафилаксии у детей раннего возраста.
Материал с сайта https://aafa.org/asthma-allergy-research/our-research/food-allergy-anaphylaxis-in-infants/
Диагностика различных форм пищевой аллергии остается сложной проблемой, международные рекомендации указывают, что единственным «золотым диагностическим стандартом» при любой форме пищевой аллергии остается провокационный оральный тест (слепой или открытый). Однако его проведение сопряжено с большими рисками, особенно если речь идет о тяжелых реакциях и анафилаксии. Поэтому в последнее время все чаще используется компонентная диагностика, которая помогает определить сенсибилизацию к аллергенным молекулам пищи.
Ниже приводим диагностический алгоритм, предложенный EAACI:
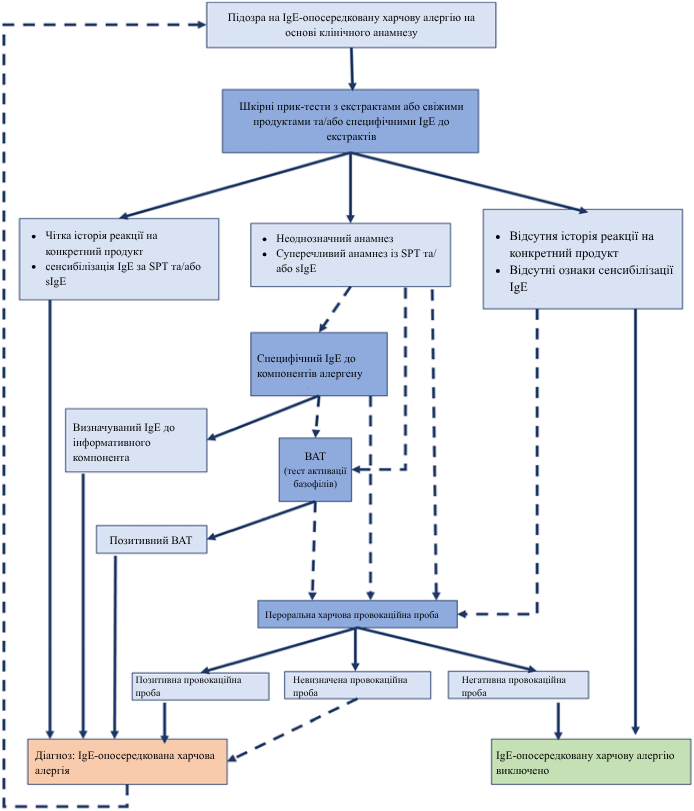
Рисунок 2 Алгоритм диагностики IgE-опосредованной пищевой аллергии
Оригинал - https://onlinelibrary.wiley.com/doi/10.1111/all.15902
Согласно рекомендациям EAACI тестами первой линии являются специфические IgE к экстракту аллергена или ШПТ, а молекулярная диагностика является тестами второй линии. EAACI не рекомендует использовать широкие панели или мультиплексные исследования как тесты первой линии из-за высокой частоты обнаружения латентной сенсибилизации.
Одним из перспективных и эффективных направлений диагностики является компонентная (молекулярная) диагностика, позволяющая определить конкретные молекулы-аллергены, обычно представленные специфическими белками.
Это имеет важное значение для:
- прогнозирования тяжести реакций;
- оценки перекрестной реактивности;
- выбора тактики лечения.
Использование монокомпонентных и многокомпонентных платформ значительно улучшает возможности диагностики при подозрении на пищевую аллергию.
Биомаркеры тяжести пищевой аллергии (таблица 3).
Прогнозирование риска анафилаксии остается важной проблемой клинической аллергологии. Перспективным маркером является базальный уровень сывороточной триптазы. Исследования показали, что повышенный уровень триптазы может быть ассоциирован с более высоким риском тяжелых анафилактических реакций. Согласно современным данным, значения ≥8 мкг/л могут быть связаны с повышенной вероятностью тяжелых реакций.
Важно, что определение триптазы рекомендуется рассматривать как инструмент стратификации риска, а не как диагностический тест аллергии.
Таблица 3.
Биомаркеры тяжести пищевой аллергии
| Биомаркер | Клиническое значение |
| Специфические IgE | Подтверждение сенсибилизации |
| Компонентная аллергодиагностика | Прогноз тяжести реакции |
| Базальный уровень сывороточной триптазы | Оценка риска тяжелой анафилаксии |
| БАТ (тест активации базофилов) | Функциональная оценка реактивности |
Менеджмент пациентов с пищевой аллергией
Для пациентов с подтвержденной пищевой аллергией ключевым компонентом менеджмента является целенаправленное обучение по избеганию аллергена, раннему распознаванию симптомов и правильному использованию эпинефрина. Следовательно, практическое консультирование должно концентрироваться прежде всего на предотвращении непреднамеренного употребления, контроле скрытых аллергенов, безопасности питания вне дома, в путешествиях, школе и заведениях общественного питания.
Эпинефрин остается препаратом первой линии при анафилаксии. Имеющиеся данные свидетельствуют, что его раннее введение ассоциировано с лучшими клиническими исходами, более низким риском бифазной реакции и меньшей потребностью в госпитализации. Задержка введения эпинефрина описывается среди факторов неблагоприятного течения, а в сериях летальных случаев лечение нередко было несвоевременным. В то же время превентивное использование эпинефрина у бессимптомного пациента после вероятного контакта с аллергеном не имеет достаточной доказательной поддержки и не должно рассматриваться как рутинная тактика. Индивидуализированный подход к пациенту является ключевым для повышения безопасности лечения.
Выводы
- Пищевая аллергия является сложной мультифакторной патологией со значительной клинической вариабельностью.
- Ключевым элементом диагностики остается детальный клинический анамнез.
- Молекулярная аллергология открывает новые возможности для персонализированной диагностики и прогнозирования риска реакций.
- Базальный уровень триптазы может использоваться как биомаркер стратификации риска тяжелых анафилактических реакций.
- Дальнейшие исследования необходимы для совершенствования алгоритмов диагностики и лечения пищевой аллергии.
Литература
- Muraro A, Worm M, et all European Academy of Allergy and Clinical Immunology, Food Allergy, Anaphylaxis Guidelines Group. EAACI guidelines: Anaphylaxis (2021 update). Allergy. 2022 Feb;77(2):357-377. doi: 10.1111/all.15032.
- EAACI guidelines on the diagnosis of IgE-mediated food allergy Alexandra F. Santos, Carmen Riggioni, Ioana Agache, at all Allergy, 2023, 78(12) https://doi.org/10.1111/all.15902
- Managing food allergy: GA2LEN guideline 2022 GA2LEN Food Allergy Guideline Group et al. World Allergy Organization Journal, Volume 15, Issue 9, 100687
- Anaphylaxis: A 2023 practice parameter update CollaboratorsWorkgroup ContributorsJoint Task Force on Practice Parameters Reviewers et al. Annals of Allergy, Asthma & Immunology, Volume 132, Issue 2, 124 – 176.
- Loli-Ausejo D, Gonzalez-Matamala MF, Martí D, Ruano-Zaragoza M, Mir-Ihara P, Solis-Ynga K, Lara R, Bartra J, Pascal M, Muñoz-Cano R. Basal Serum Tryptase Outperforms Hereditary Alpha Tryptasemia as a Biomarker of Food Allergy Severity. Allergy. 2025 Aug;80(8):2376-2378. doi: 10.1111/all.16623.
- Tedner SG, Asarnoj A, et all Food allergy and hypersensitivity reactions in children and adults-A review. J Intern Med. 2022 Mar;291(3):283-302. doi: 10.1111/joim.13422.
- Loprinzi Brauer CE, Motosue MS, Li JT, Hagan JB, Bellolio MF, Lee S, Campbell RL. Prospective Validation of the NIAID/FAAN Criteria for Emergency Department Diagnosis of Anaphylaxis. J Allergy Clin Immunol Pract. 2016 Nov-Dec;4(6):1220-1226. doi: 10.1016/j.jaip.2016.06.003.








