
Аллергия на пшеницу: современный подход к диагностике
17.07.2025
Распространенность глютена в рационе человека
Зерновые культуры, содержащие глютен, стали фундаментальной частью рациона человека, а пшеница является наиболее потребляемой злаковой культурой в мире [Publishing, O. OECD-FAO Agricultural Outlook 2019–2028; Organisation for Economic Co-Operation and Development OECD: Rome, Italy, 2019]. Ее широкое использование в пищевой промышленности подчеркивает значение пшеницы как важного питательного компонента [Al-Toma, A.; Volta, U.; Auricchio, R.; Castillejo, G.; Sanders, D.S.; Cellier, C.; Mulder, C.J.; Lundin, K.E. European Society for the Study of Coeliac Disease (ESsCD) Guideline for Coeliac Disease and Other Gluten-Related Disorders. United Eur. Gastroenterol. J. 2019, 7, 583–613].
Глютен, состоящий преимущественно из запасных белков, является основным структурным белком пшеницы. Побочные реакции на употребление глютена классифицируются по трем основным патофизиологическим механизмам:
1. Аутоиммунные реакции, например, целиакия (ЦЛ).
2. Неаутоиммунные и неаллергические реакции, примером которых является нецелиакическая чувствительность к глютену (NCGS).
3. Аллергические причины.
Аллергические реакции могут быть вызваны IgE-опосредованными, смешанными IgE/не-IgE-опосредованными и не-IgE-опосредованными механизмами.
Пшеница как аллерген и связанные с ней клинические проявления
В последние годы пшеница (Triticum spp.) получила признание как значимый пищевой аллерген, стоящий в одном ряду с такими известными аллергенами, как коровье молоко, яйца, соя и арахис.
Пищевая аллергия на пшеницу характеризуется выработкой IgE-антител к белкам пшеницы и развитием симптомов немедленного типа. Хотя в целом аллергия на пшеницу является относительно редким явлением, в некоторых регионах, в частности в частях Азии (включая Японию и Таиланд), она стала основной причиной пищевой аллергии. [Srisuwatchari W, Vichyanond P (2018) Oral food challenges: result of a 16-year experience at a major teaching hospital in Thailand. Asia Pac Allergy 8:e21].
При IgE-опосредованных реакциях клиническая картина может варьироваться от легких кожно-слизистых проявлений, таких как крапивница и/или ангионевротический отек, до угрожающей жизни анафилаксии. Важно отметить, что хотя Т-клетки играют центральную роль в патофизиологии атопического дерматита (АД) и эозинофильных желудочно-кишечных расстройств, значительная подгруппа пациентов также демонстрирует сопутствующие IgE-опосредованные механизмы. Такие реакции классифицируются как смешанные IgE/не-IgE-опосредованные. Не-IgE-опосредованные реакции, в свою очередь, преимущественно поражают желудочно-кишечный тракт, проявляясь как синдром энтероколита, индуцированного пищевым белком (FPIES), или энтеропатия, индуцированная пищевым белком.
Уникальные формы аллергии на пшеницу: WDEIA и WANDA
IgE-опосредованный механизм также охватывает уникальное состояние, известное как анафилаксия, индуцированная физическими упражнениями, зависимая от пшеницы (WDEIA). Это отдельная клиническая единица, при которой анафилаксия возникает только в том случае, когда после употребления пшеницы происходит физическая нагрузка.
Последние исследования показывают, что другие кофакторы, такие как нестероидные противовоспалительные препараты (НПВП) или алкоголь, также могут усиливать реакции, а в некоторых случаях даже провоцировать симптомы при отсутствии физических упражнений. Эта более широкая клиническая картина получила название аллергия на пшеницу, зависимая от факторов аугментации (WANDA).
Были предложены различные механизмы для объяснения того, как физические упражнения действуют как кофактор при WDEIA, однако подтверждающие данные остаются ограниченными. Это подчеркивает необходимость дальнейших исследований для выяснения основной патофизиологии этих состояний. Заметным примером, демонстрирующим сложность аллергии на пшеницу, является вспышка аллергической контактной крапивницы, анафилаксии и/или WDEIA в Японии, связанная с использованием мыла для лица, содержащего специфический тип гидролизованного пшеничного белка [Yagami A, Aihara M, Ikezawa Z, Hide M, Kishikawa R, Morita E et al (2017) Outbreak of immediate-type hydrolyzed wheat protein allergy due to a facial soap in Japan. J Allergy Clin Immunol 140:879-881.e877].
Классификация белков пшеницы и их аллергенная значимость
Белки пшеницы можно классифицировать на две основные категории:
- Водорастворимые (альбумины)/солерастворимые (глобулины).
- Спирто-/водорастворимые (мономерные глиадины) и растворимые в разбавленной кислоте (полимерные глютенины).
К группе водо/солерастворимых белков относятся ингибиторы альфа-амилазы (AAI, Tri a 15), белки переноса липидов (LTP, Tri a 14) и авениноподобные белки.
Глиадины, которые являются спирто/водорастворимыми, делятся на:
- альфа (α)/бета (β)-глиадин (Tri a 21)
- гамма (γ)-глиадин (Tri a 20)
- омега (ω)-5-глиадин (Tri a 19)
Глютенины, растворимые в разбавленной кислоте, состоят из высокомолекулярного глютенина (HMW, Tri a 26) и низкомолекулярного глютенина (LMW, Tri a 36).
Наиболее аллергенными белками пшеницы, ответственными за IgE-опосредованную аллергию на пшеницу, являются глиадины, в частности ω-5-глиадин, и глютенины. В случаях анафилаксии, индуцированной физическими упражнениями, зависящей от пшеницы (WDEIA), ω-5-глиадин и LTP были определены как основные аллергены.
Перекрестная реактивность белков злаковых культур
Глиадины и глютенины, которые являются основными запасными белками в зернах пшеницы, относятся к семейству проламинов злаков (глютен). Проламины пшеницы демонстрируют значительную степень гомологии последовательности и структуры с аналогичными белками в других злаковых, таких как ячмень (гордеины), рожь (секалины), овес (авенины) и кукуруза (коиксины), а также, в меньшей степени, с некоторыми видами трав. Эта гомология приводит к значительной перекрестной реактивности in vitro между этими зерновыми культурами. Однако клиническая перекрестная реактивность, как правило, вызывает меньшее беспокойство.
В странах, где пыльца злаков является основной причиной сенсибилизации у пациентов с аллергией, перекрестная реактивность между тимофеевкой и пшеницей является распространенным явлением. Эта перекрестная реактивность включает два известных аллергена, присутствующих как в пшенице, так и в пыльце трав: углеводные детерминанты (CCD) и профиллины. У таких пациентов обычно наблюдается низкий уровень специфических IgE к пшенице (sIgE) и они остаются бессимптомными.
Исследование Нильссона и соавторов (2018) Nilsson N, Nilsson C, Ekoff H, Wieser-Pahr S, Borres MP, Valenta R et al (2018) Grass-allergic children frequently show asympto- matic low-level IgE co-sensitization and cross-reactivity to wheat. Int Arch Allergy Immunol 177:135–144. https://doi.org/10.1159/ 000489610] показало, что 43 из 72 детей (59,7%) с диагностированной врачом аллергией на пыльцу трав были сенсибилизированы к пшенице, со средним уровнем sIgE 0,5 kUA/l. Это подчеркивает важность понимания потенциальной, хотя часто бессимптомной, перекрестной сенсибилизации у пациентов с аллергией на пыльцу злаков.
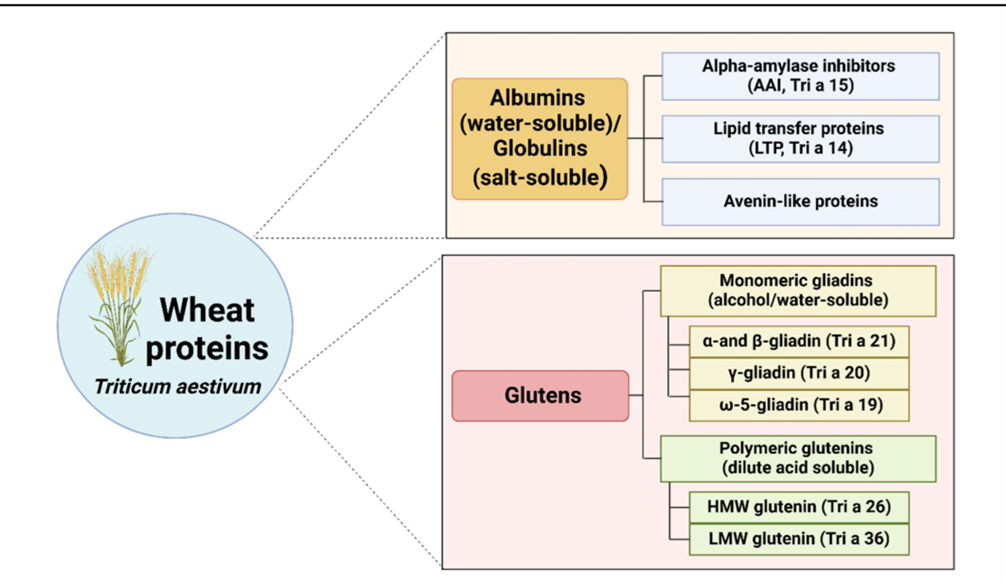
Рис. 1. Основные аллергены белка пшеницы. Создано BioRender.com/Mahidol University (дата обращения: 31 января 2025 г.) [Clinical Reviews in Allergy & Immunology (2025) 68:47]
Диагностика IgE-опосредованной аллергии на пшеницу
Диагностика IgE-опосредованной аллергии на пшеницу традиционно основывается на тщательном клиническом анамнезе в сочетании с кожными прик-тестами (ШПТ) и/или измерением сывороточного специфического IgE (sIgE).
Для повышения точности диагностики критически важным является определение sIgE к компонентам пшеницы, а именно:
- rTri a 19 (омега-5 глиадин): считается главным аллергеном пшеницы и является маркером истинной сенсибилизации к пшенице.
- rTri a 14.
Исследование на пищевые sIgE широко доступны в клинической практике и обычно используются для диагностики аллергии на пшеницу. Они также могут помочь спрогнозировать тяжесть реакций. Однако положительные результаты sIgE всегда следует интерпретировать с учетом клинического анамнеза, поскольку положительный результат при отсутствии клинических симптомов указывает только на сенсибилизацию без клинического значения. В настоящее время ImmunoCAP, флуоресцентный метод, является стандартом для количественного определения sIgE.
Молекулярная аллергодиагностика для уточнения аллергенов пшеницы
Для идентификации специфических аллергенов пшеницы, таких как ω-5-глиадин, и повышения диагностической точности была разработана молекулярная аллергодиагностика. Метод флуоресцентного иммуноферментного исследования (FEIA) ImmunoCAP® позволяет идентифицировать ограниченный спектр аллергенов пшеницы, в частности глиадин, ω-5-глиадин (Tri a 19) и неспецифический белок переноса липидов (ns-LTP, Tri a 14).
Учитывая, что ω-5-глиадин является основным аллергеном при IgE-опосредованной аллергии на пшеницу, определение уровня ω-5-глиадин-sIgE может обеспечить более точный диагноз, чем общий sIgE к пшенице.
Вызовы и оптимизация диагностики аллергии на пшеницу
Следует отметить, что точность диагностики аллергии на пшеницу все еще ниже по сравнению с другими распространенными пищевыми аллергенами. Как следствие, постановка точного диагноза может быть сложной и часто требует проведения перорального пищевого провокационного теста (ППТ). Этот метод является трудоемким и несет значительные риски, особенно для детей младшего возраста. Поэтому критически важным является выбор подходящего метода и оборудования для диагностических исследований.
ДІЛА предлагает оптимальный вариант исследований, проводимых с помощью метода ImmunoCAP. Этот метод обеспечивает высокую точность благодаря:
- Высокой воспроизводимости результатов: Количественное определение специфических IgE-антител, подтвержденное более чем 5000 международными научными публикациями.
- Полной автоматизации процесса: Исключение человеческого фактора и минимизация возможных погрешностей.
Значение молекулярного пакета "Пшениця"
Молекулярный пакет «Пшеница» от ДІЛА позволяет определить сенсибилизацию к аллергокомпоненту пшеницы rTri a 19 (омега-5 глиадин). Это является ключевым показателем истинной пищевой аллергии на пшеницу и помогает прогнозировать тяжелые аллергические реакции при употреблении пшеницы и наличии кофакторов (например, WDEIA-синдром).
Кроме того, выявление сенсибилизации к компоненту пшеницы Tri a 14 полезно для дифференциальной диагностики перекрестных реакций с другими растительными аллергенами и для доказательного обоснования необходимости исключения пшеницы из рациона.
Выводы
Аллергия на пшеницу, являющаяся комплексным и многогранным иммунным ответом, представляет собой значительный диагностический вызов в клинической практике. В отличие от целиакии или нецелиакической чувствительности к глютену, истинная аллергия на пшеницу характеризуется IgE-опосредованными механизмами и может проявляться от легких кожно-слизистых реакций до угрожающих жизни анафилаксии, включая уникальные явления, такие как анафилаксия, индуцированная физическими упражнениями, зависимая от пшеницы (WDEIA) и аллергия на пшеницу, зависимая от факторов аугментации (WANDA).
Точная диагностика требует сочетания подробного клинического анамнеза и измерения специфических IgE-антител. В частности, молекулярная аллергодиагностика, определяющая IgE к ключевым аллергокомпонентам пшеницы, таким как ω-5-глиадин (rTri a 19) и Tri a 14, значительно повышает точность и позволяет дифференцировать истинную аллергию на пшеницу от перекрестных реакций (например, с пыльцой злаков).
Применение высокоточных методов, таких как ImmunoCAP, которые обеспечивают количественное определение специфических IgE-антител и минимизируют влияние человеческого фактора благодаря полной автоматизации, является критически важным для получения надежных результатов. Это позволяет врачам не только подтвердить диагноз, но и прогнозировать потенциальную тяжесть реакций, что является основой для эффективного управления состоянием пациента и разработки индивидуальных рекомендаций по элиминационной диете.








