
Клинико-лабораторный менеджмент диагностики целиакии
27.10.2022
Что мы знаем о распространенности целиакии? Основываясь на европейских и американских серологических скрининговых исследованиях, считается, что бессимптомная целиакия наблюдается с частотой 1/100-300, а симптомная ~1/3 345. Встречается в 2 раза чаще у женщин, чем у мужчин. Однако до сих пор открытым остается вопрос недиагностированной целиакии. Об актуальных проблемах диагностики и лечения целиакии рассказала Солдатова Оксана Владимировна – к. мед. н., доцент кафедры детских и подростковых заболеваний Национального университета здравоохранения Украины имени П.Л. Шупика, эксперт ДОЗ КГГА, вице-президент Независимой Ассоциации нутрициологов и диетологов Украины во время симпозиума opinion leaders нутрициологии и диетологии с международным участием «Можно ли сохранить оптимальное питание в обычных и экстремальных условиях?».
Разнообразие симптомов, возникающих вследствие повреждения многих органов в связи с нарушением функции тонкого кишечника, а также частое сочетание целиакии с другими аутоиммунными заболеваниями, является причиной недиагностированной целиакии, хотя возможности медицины позволяют ее определить. В медицинской среде до сих пор бытуют мифы по диагностике целиакии:
Миф 1: Выявление болезни возможно только в младенческом возрасте
Миф 2: Целиакия сопровождается гастроинтестинальными симптомами:
- хроническая или периодическая диарея,
- хронический запор,
- хронические боли в животе,
- метеоризм,
- периодической тошноты,
- периодической рвоты.
Миф 3: для диагностики целиакии обязательно определение только иммуноглобулинов к глиадину.
На самом деле целиакию можно диагностировать в любом возрасте (у взрослого) и очень часто она имеет внеинтестинальные симптомы, а именно:
- потерю веса,
- недостаточный привес у детей,
- задержку роста (или низкий рост),
- задержку полового созревания,
- аменорею,
- раздражительность,
- хроническая усталость,
- нейропатию,
- артрит (или артралгию),
- хроническую железодефицитную анемию,
- снижение минерализации костей (остеопения/остеопороз),
- повторные переломы,
- рецидивирующий афтозный стоматит,
- герпетиформный дерматит,
- дефекты зубной эмали,
- аномальную биохимию печени (увеличение АЛТ, АСТ),
- симптомы болезни могут отсутствовать.
Важную роль в диагностике играет определение иммуноглобулинов к тканевой трансглютаминазе, эндомизии и дезаминированному глиадину. Рекомендуется также пройти генетическое тестирование для исключения или подтверждения целиакии.
Что же такое целиакия? Целиакия – это генетически детерминированное аутоиммунное заболевание с преимущественным поражением тонкого кишечника, которое связано с употреблением в пищу глютена. Глютен - группа белков: проламина и глютенина, входящих в состав: зерновых злаков (пшеница, рожь, ячмень, овес), родственных видов пшеницы (полба, хорасан, эммер, эйнкорн, тритикале, спельта). Проламины: пшеница (глиадин), ячмень (гордеин), рожь (секалин), овес (авенин) придают тесту эластичность и упругость. Например: в состав белков пшеницы входят: глиадина 40%, глютенины 40%, альбумины-10%, глобулины – 10%. Аутоиммунное воспаление слизистой тонкого кишечника – целиакия – вызывает нарушение всех его функций, а именно пищеварения, усвоения, секреторной и двигательной деятельности.
Важно отметить, что если в рационе присутствует глютен, иммунная система больного целиакией находится под постоянным антигенным давлением, вследствие чего могут возникать другие аутоиммунные заболевания. Под влиянием глютена образуются специфические антитела (к тканевой трансглютаминазе типа 2 [tTG], антиэндомизиальные [EMA], к дезаминированным пептидам глиадина [DGP]) и развивается аутоиммунная воспалительная реакция, которая приводит к атрофии ворсинок слизистой оболочки тонкого кишечника.
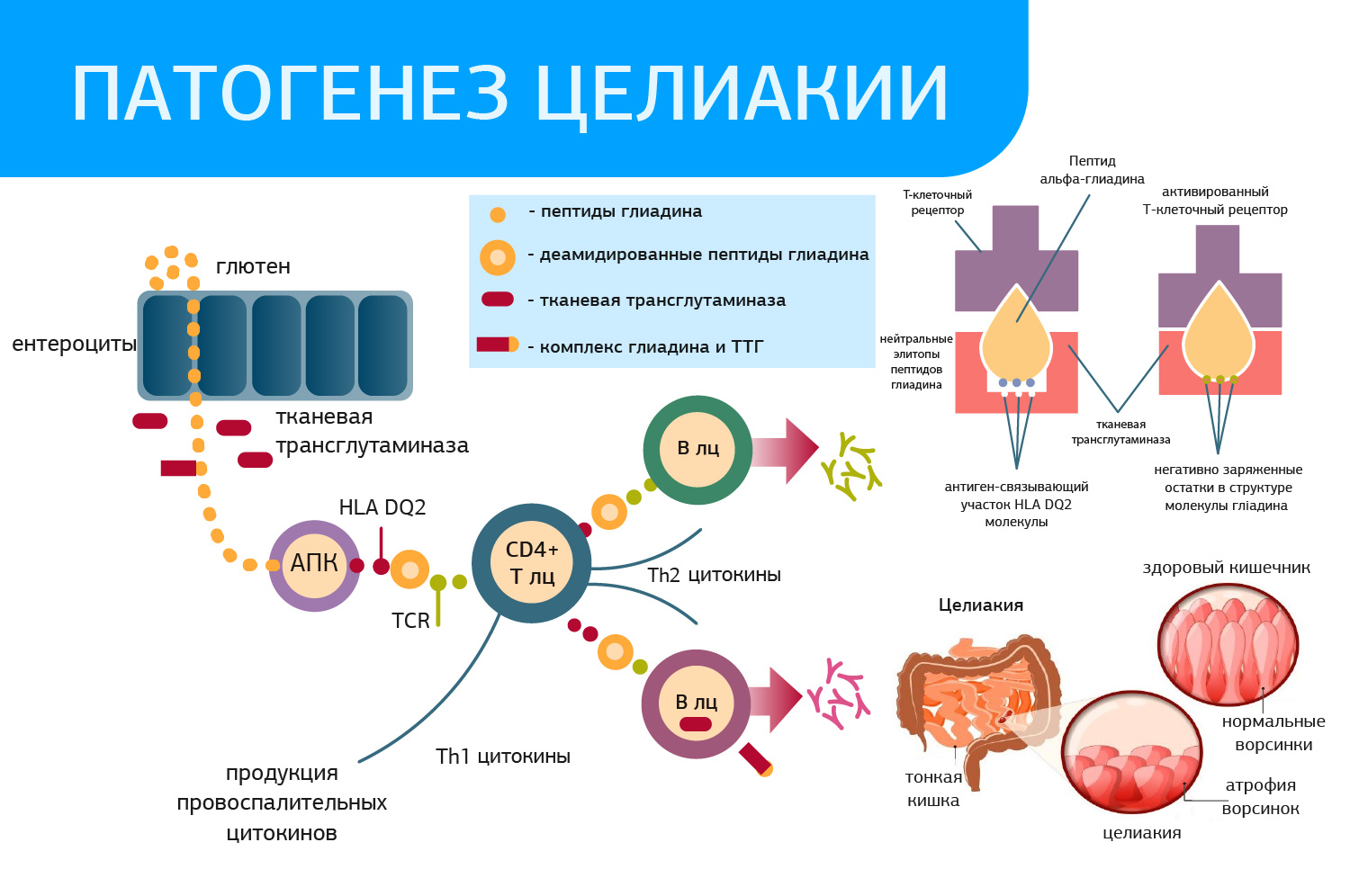
Антитела можно обнаружить в ≈1% от общей популяции; риск целиакии повышен у больных сахарным диабетом 1-го типа, аутоиммунными заболеваниями печени и/или щитовидной железы, с синдромом Дауна, с синдромом Шерешевского-Тернера, с синдромом Уильямса, с нефропатией IgA, с дефицитом IgA и у родственников 1-й степени, больных целиакией.
Важное влияние на развитие Целиакии оказывают факторы окружающей среды, т.е.
1. Состав микробиоты кишечника (гестационный возраст при рождении ребенка, тип вскармливания, кишечные инфекции, антибактериальные препараты):
- уменьшение гидролиза глютена в просвете кишечника,
- увеличение кишечной проницаемости,
- влияние на стимуляцию врожденного и обретенного иммунитета.
2. «Молекулярная мимикрия» между белками вирусов, бактерий или кандид и глиадином:
- Ротавирус (триггер аутоиммунного воспаления (Ig А до tTG2) и увеличение кишечной проницаемости вследствие энтерита),
- Candida albicans (стимулирование синтеза Ig А к tTG2).
Целиакию делят на:
- Классическую
- Неклассическую
- Бессимптомную
- Потенциальную
- Рефрактерна
- Сероотрицательную
Проявления классической целиакии:
- Потеря веса
- Задержка роста
- Задержка полового развития
- Рвота
- Хроническая диарея
- Растяжение живота вследствие метеоризма
- Железодефицитная анемия
- Снижение мышечной массы
- Отеки вследствие гипопротеинемии
- Раздражение и депрессивное настроение
Проявления неклассической целиакии:
- Абдоминальная боль
- Целиакционный криз (холероподобный синдром)
- Хроническая усталость
- Хронический запор у детей
- Диспепсия, ранняя насыщенность, анорексия
- Головная боль, хроническая мигрень
- Дерматологические проявления (сыпь, псориаз, пузырьки)
- Алопеция
- Периферическая нейропатия, атаксия
- Беспричинное повышение АЛТ, АСТ
- Дефицит фолиевой кислоты
- Дефицит витамина B12
Могут быть симптомы: снижение плотности костей (остеопения, остеопотроз), артриты, артралгии, беспричинное бесплодие, задержка пубертатного периода, позднее менархе/ранняя менопауза, беспричинные выкидыши, преждевременные роды или депрессия, новорожденный и тревожность, изменение настроения и раздражительность.
Проявления потенциальной целиакии:
- есть генетический риск (HLA-DQ2/DQ8)
- есть аутоантитела к tТG и ЭМА
- при употреблении глютена не развивается атрофия ворсинок тонкого кишечника, или ее проявления незначительны.
Проявления рефрактерной целиакии:
- персистенция или рецидивирование клинических симптомов и гистологических изменений СО тонкого кишечника в течение 12 месяцев при соблюдении БГД. (СО-слизистая, БГД- безглютеновая диета).
Выделяют определенные причины персистенции симптомов целиакии: употребление скрытого глютена, ложный диагноз целиакии, сопутствующий СПК, лактазная недостаточность, пищевая аллергия на другие продукты, панкреатическая недостаточность, микроскопический колит, синдром избыточного бактериального роста, воспалительные заболевания, энтеропатией.
Проявления сероотрицательной целиакии:
- отсутствие специфических серологических маркеров
- наличие клинических симптомов тяжелой мальабсорбции
- наличие атрофии ворсинок тонкого кишечника при биопсии
Диагностика
Для диагностики целиакии используются разные подходы (анамнез, клиническое обследование, серология, генетическое тестирование, гистопатологические исследования), но ни один из них не может считаться достаточным для установления диагноза. Диагностика достоверна только при предварительном ежедневном (в течение ≥6-ти нед.) потреблении ≥1-го блюда, содержащего глютен (≈10 г глютена в день — столько содержат 4 ломтика хлеба).
Показания к серологической диагностике:
- скрининговое исследование у пациентов с подозрением на целиакию (отбор для биопсии тонкого кишечника);
- скрининговое исследование в группах повышенного риска заболеваемости целиакией;
- оценка соблюдения безглютеновой диеты.
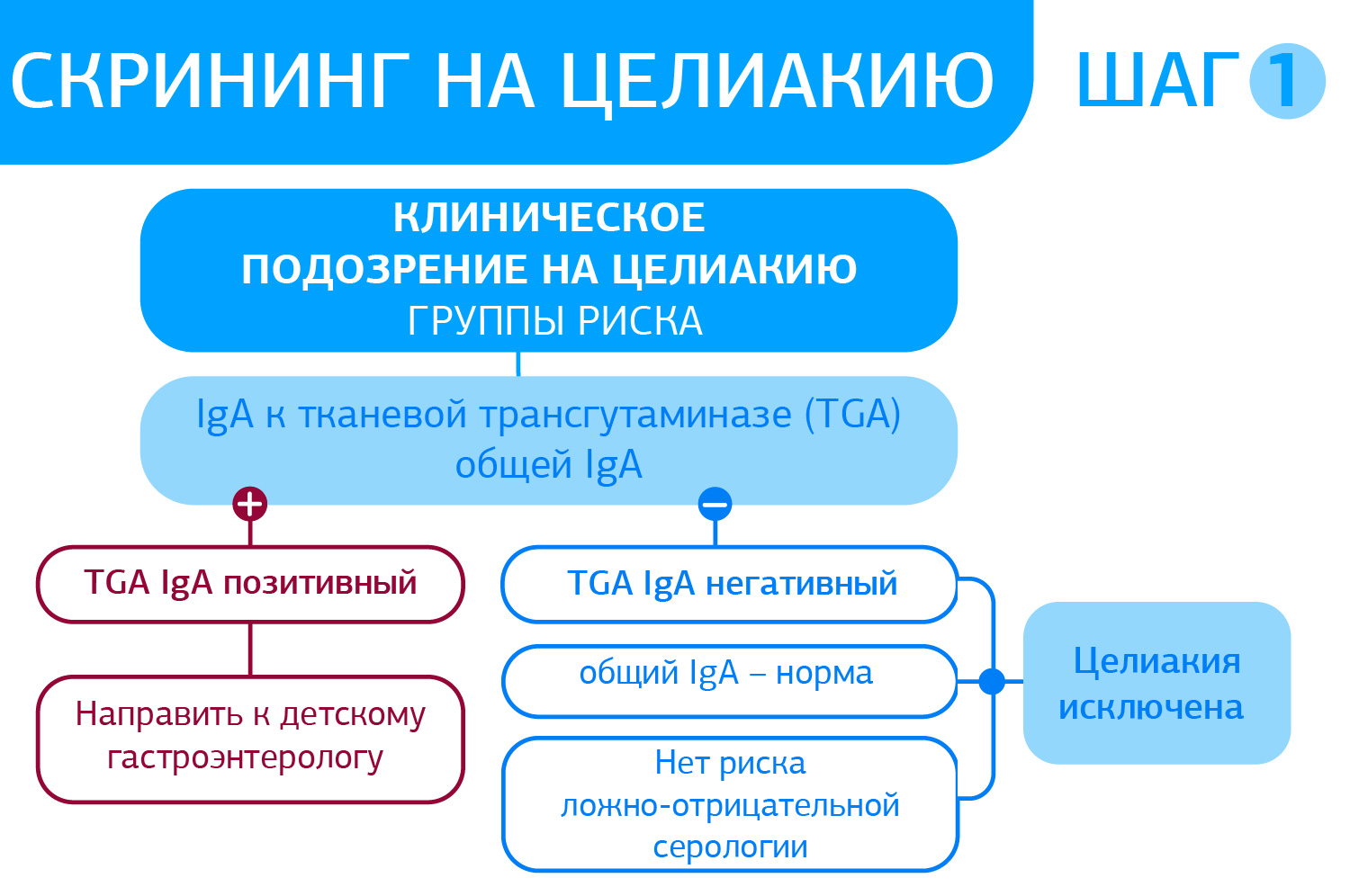
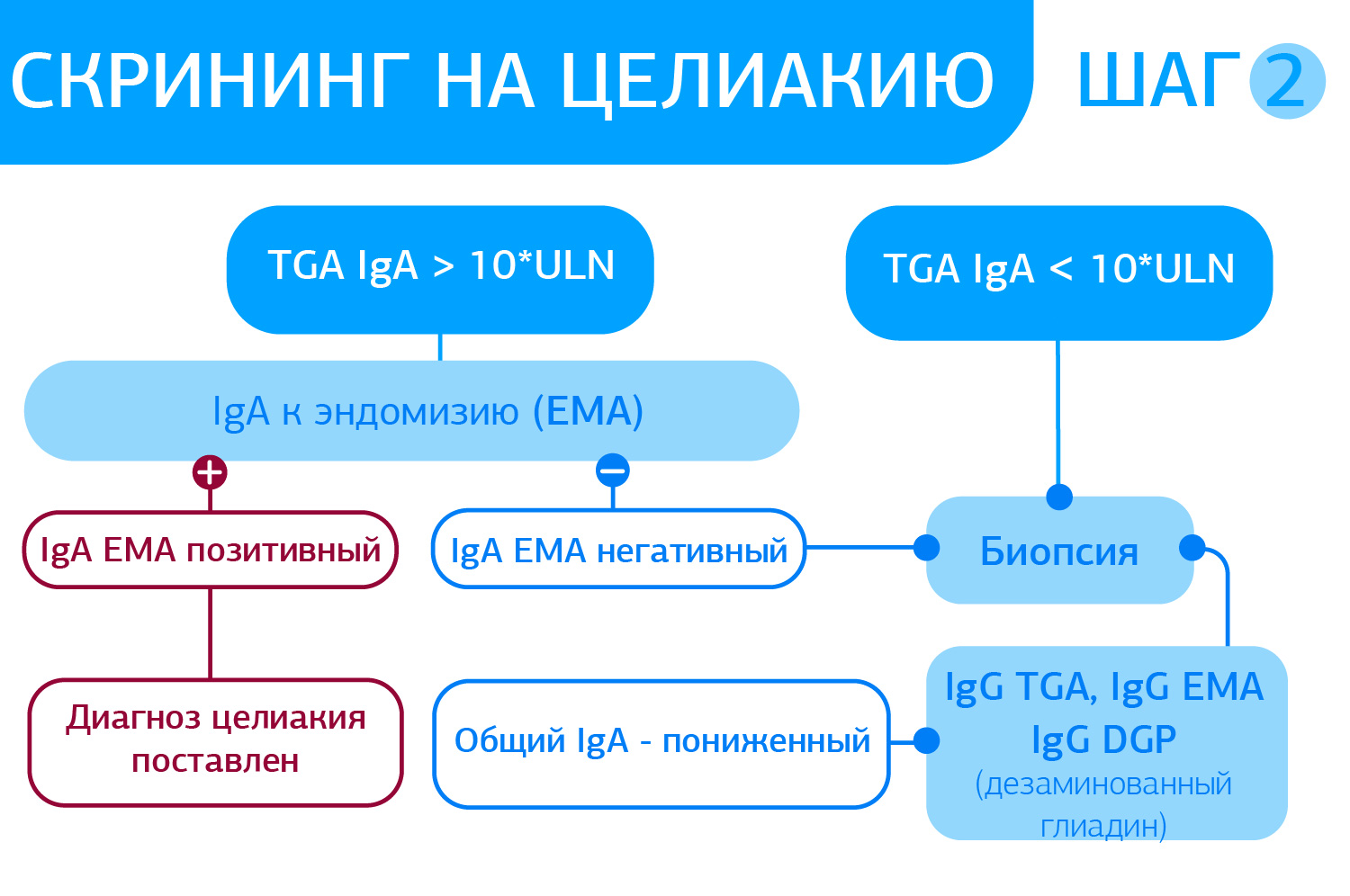
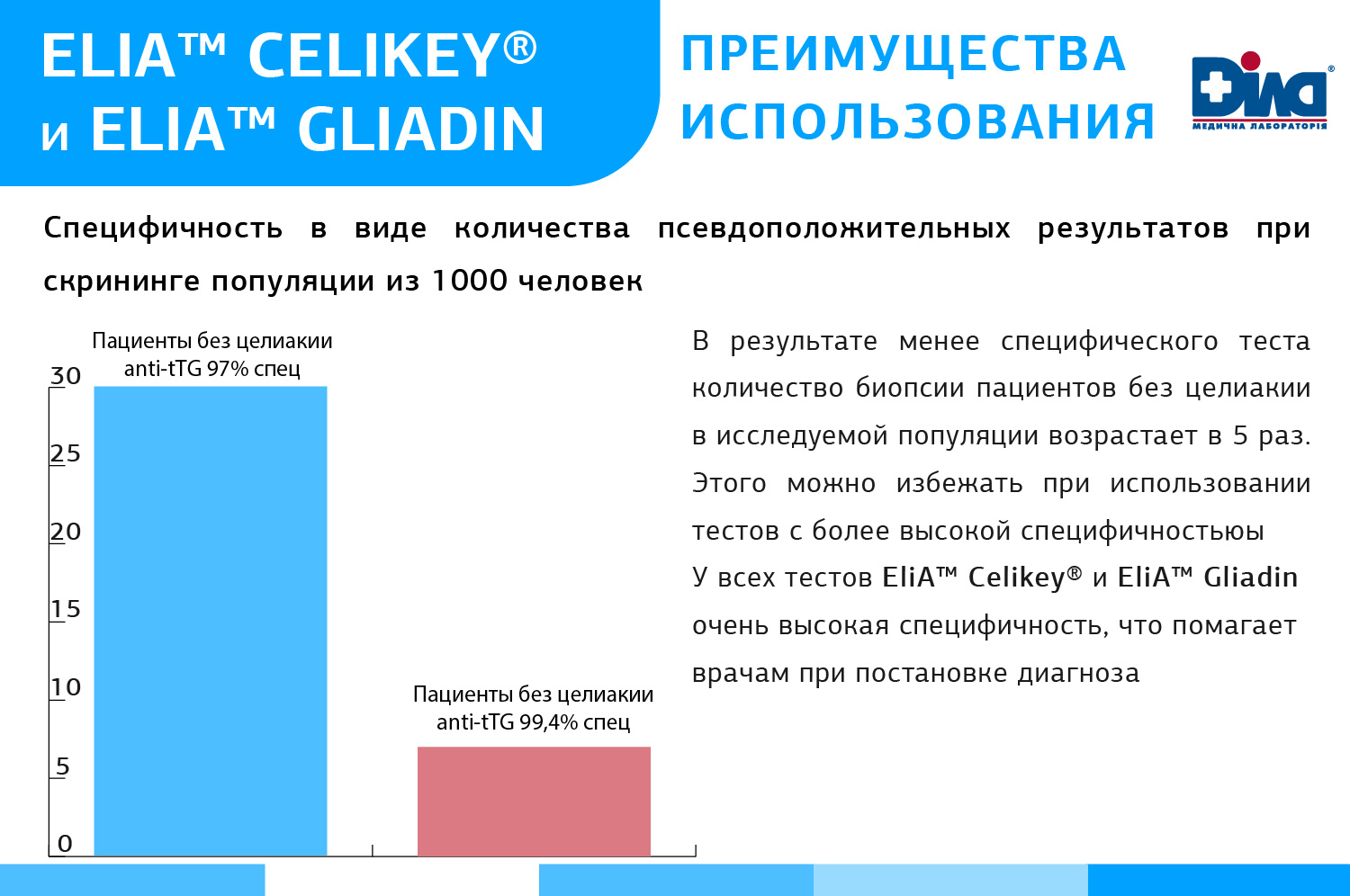
Алгоритм серологической диагностики ГЛС от ДІЛА базируется на тестах ВТОРОГО ПОКОЛЕНИЯ, что соответствует мировым и Европейским тенденциям диагностики. Основные преимущества диагностики Целиакии – специфичность и чувствительность тестов EliA™ Celikey® и EliA™ Gliadin. (См. ниже)

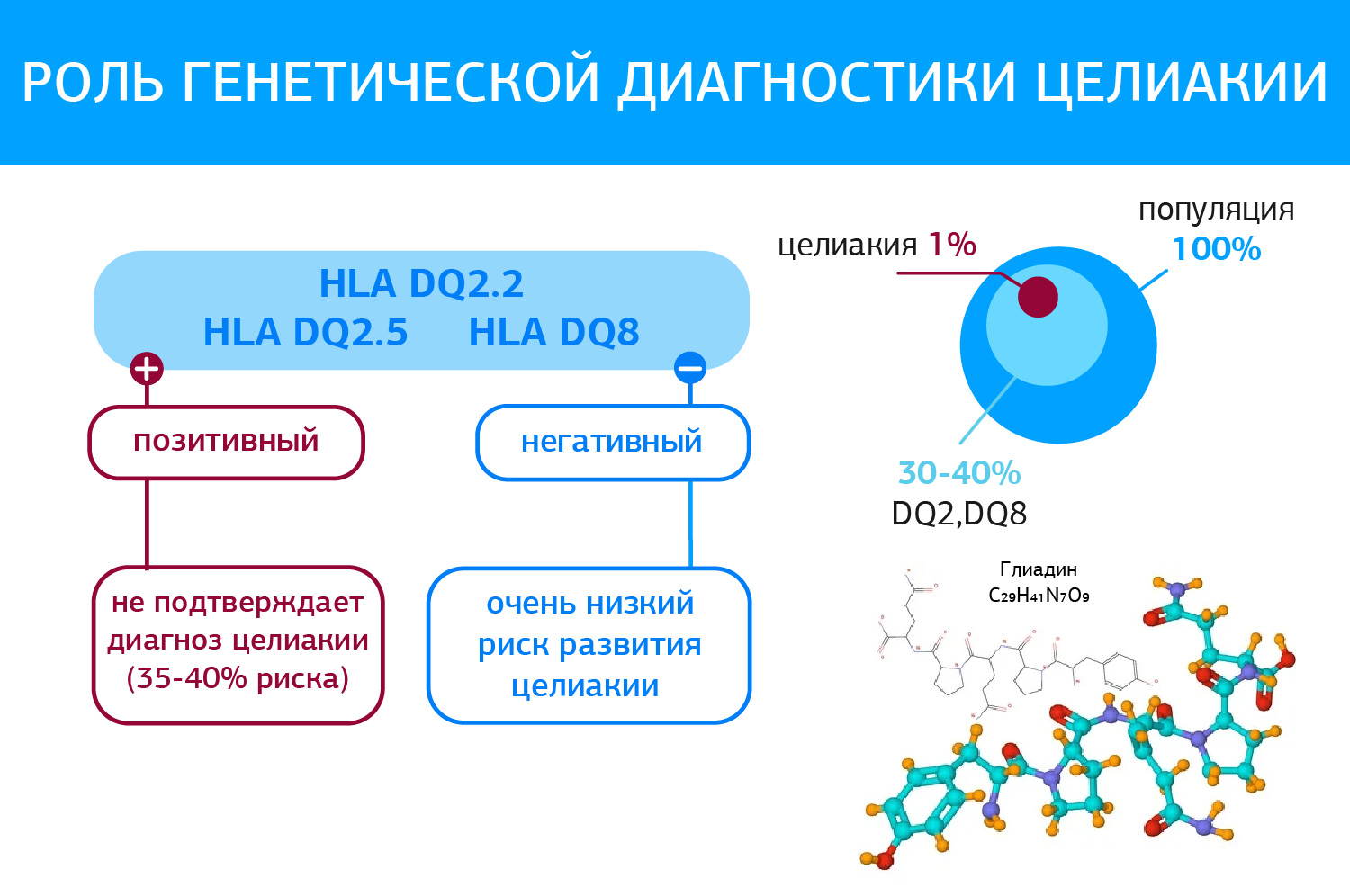
Роль генетической диагностики целиакии:
Генетические исследования исключают, а не подтверждают диагноз, поскольку 35-40% популяции являются носителями генов, ассоциированных с целиакией, согласно рекомендациям (Al-Toma A, Volta U, Auricchio R, et al. European Society for Study of Coeliac Disease ((ESsCD) guideline for coeliac disease and other gluten-related disorders. United European Gastroenterol J. 2019; У пациентов с подтвержденной целиакией определяются HLA-DQ2.5 – в 90-95%, а HLA-DQ2.2 и HLA-DQ8 – в 5-10%. Отсутствие генотипов HLA-DQ2 или DQ8 исключает диагноз целиакии.
Таким образом:
- Тестирование HLA-DQ2/DQ8 не должно использоваться рутинно при первичной диагностике целиакии (сильная рекомендация, средний уровень доказательности)
- Тестирование HLA-DQ2/DQ8 необходимо проводить для исключения целиакии в отдельных клинических случаях:
• Гистология Марш 1-2 у серонегативных пациентов;
• у пациентов, которым назначена БГД без серологического скрининга на целиакию;
• в случаях, когда результаты специфической серологии положительны, а гистологические признаки целиакии отсутствуют (Сильная рекомендация, средний уровень доказательности).
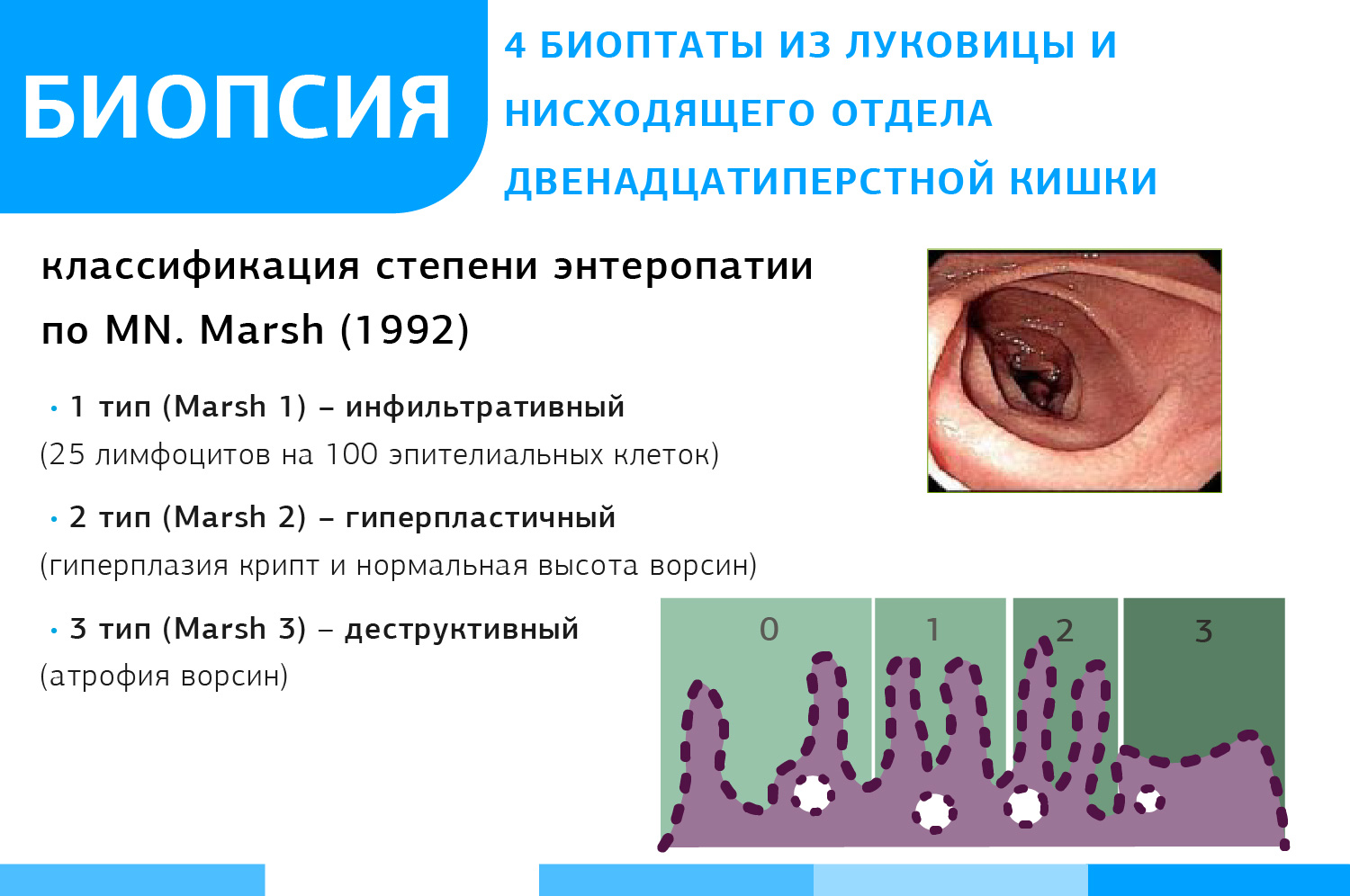
Гистологическое исследование слизистой тонкого кишечника в диагностике целиакии имеет основное значение. Забор биоптатов проводят из двенадцатиперстной кишки (1-2 из луковицы и 4-х из внелукового отдела). Характерным гистологическим признаком является атрофия кишечных ворсинок, сопровождающаяся увеличением количества эндоэпителиальных лимфоцитов и гипертрофией крипт.
Указаны определенные шаги диагностики Целиакии у пациентов, уже соблюдающих БГД (безглютеновую диету) Al-Toma A, Volta U, Auricchio R, et al. European Society for Study of Coeliac disease (ESsCD) guideline для coeliac disease and other gluten-related disorders. United European Gastroenterol J. 2019; 7(5): 583-613. doi:10.1177/2050640619844125:
1. Серологическое тестирование положительное, следующий шаг – биопсия из тонкого кишечника.
2. Серологическое тестирование отрицательное, а генетическое (HLA DQ2/DQ8) положительное – необходимо проводить пробу на глютен (сильная рекомендация, высокий уровень доказательности).
К осложнениям целиакии относятся:
- рак (риск снижается почти до нормальных показателей через 5 лет соблюдения БГД)
- злокачественные лимфомы
- аденокарцинома тонкого кишечника
- орофарингеальные опухоли
- беспричинное бесплодие (12%)
- поражение костей и нарушение роста (остеопороз 30–40%)
- переломы костей (35% для пациентов с классической целиакией)
- у взрослых повышен риск смерти
- патологическая беременность и роды
Прогноз при соблюдении пациентами безглютеновой диеты благоприятный: наблюдается значительное улучшение состояния, исчезновение симптомов и повышение качества жизни, также снижается риск, как доброкачественных, так и злокачественных осложнений.
Какие врачебные ошибки имеют место при постановке диагноза целиакия?
Врач для диагностики целиакии назначил обследование:
- после начала безглютеновой диеты
- только Ig G/A к глиадину
- без учета иммунодефицитных состояний
- генетическую диагностику для подтверждения диагноза
- биопсию без серологической диагностики
При дифференциальной диагностике глютеновой болезни (целиакии) нужно исключить определенную патологию ЖКТ, а именно: язвенную болезнь желудка и 12-типерстной кишки, хронический гастрит ассоциированный с Хеликобактером пилори, атрофический гастрит, нарушение всасывания (мальабсорбция) заболеваниями желудка. Для такой дифдиагностики ДІЛА предлагает «Гастрокомплекс» – комплексное исследование крови, включающее такие маркеры как:
- пепсиноген I и II,
- соотношение пепсиноген I к пепсиноген II,
- гастрин-17 количествен.,
- Хеликобактериоз,
- Helicobacter pylori,
- Антитела IgG.
Измерение концентраций вышеперечисленных биомаркеров позволяет врачу провести косвенную оценку состояния слизистой желудка и спланировать дальнейшие шаги. На основании полученных результатов всех пациентов с диспепсией делят на три группы:
- Пациенты с нормальной слизистой желудка
- Пациенты с Хеликобактериозом без атрофического гастрита
- Пациенты с атрофическим гастритом
Исследование используется для оценки состояния слизистой желудка:
- Как безопасный неинвазивный метод диагностики, позволяющий выявить причину диспепсических расстройств (тошнота, изжога, боль в желудке);
- Высокоспецифический первоначальный метод диагностики для пациентов с противопоказаниями к инструментальным методам обследования (ЭФГДС и др.);
- Оптимальный скрининговый метод оценки слизистой желудка и раннего выявления атрофического гастрита;
- Для дополнительной информации врачу-эндоскописту при диагностике предраковых изменений слизистой желудка
Важно знать, что Гастрокомплекс – это косвенный метод оценки состояния слизистой желудка, который не может полностью заменить гастроскопию.
При подготовке к исследованию необходимо учитывать прием ингибиторов протонной помпы – пантопразола, омепразола и др., антацидов, Н2-блокаторов.
Используемые источники:
- Niland B., Cash B.D. Health benefits and adverse effects of a gluten-free diet in non-celiac disease patients. Gastroenterol Hepatol (NY) 2018; 14: 82-91.
- Golley S., Corsini N., Topping D. et al. Motivations for avoiding wheat consumption in Australia: results from a population survey. Public Health Nutr 2015; 18: 490-499.
- ESPGHAN Guidelines for Diagnosing Coeliac Disease, 2019,2020
- Lebwohl B., Sanders D.S., Green P.H.R. Coeliac disease. Lancet 2018; 391: 70-81.
- Catassi C., Alaedini A., Bojarski C. et al. The overlapping area of non-celiac gluten sensitivity (NCGS) and wheat-sensitive irritable bowel syndrome (IBS): an update. Nutrients 2017; 9:pii: E1268.
- Tanpowpong P., Ingham T.R., Lampshire P.K. et al. Coeliac disease and gluten avoidance in New Zealand children. Arch Dis Child 2012; 97: 12-16.
- Aziz I., Lewis N.R., Hadjivassiliou M. et al. A UK study assessing the population prevalence of self-reported gluten sensitivity and referral characteristics to secondary care. Eur J Gastroenterol Hepatol 2014; 26: 33-39.
- Carroccio A., Giambalvo O., Blasca F. et al. Self-reported non-celiac wheat sensitivity in high school students: demographic and clinical characteristics. Nutrients 2017; 9: pii: E771.
- Volta U., Tovoli F., Cicola R. et al. Serological tests in gluten sensitivity (nonceliac gluten intolerance). J Clin Gastroenterol 2012; 46: 680-685.
- Carroccio A., Mansueto P., Iacono G. et al. Nonceliac wheat sensitivity diagnosed by double-blind placebo-controlled challenge: exploring a new clinical entity. Am J Gastroenterol 2012; 107: 1898-1906.
- Lovell R.M., Ford A.C. Global prevalence of and risk factors for irritable bowel syndrome: a meta-analysis. Clin Gastroenterol Hepatol 2012; 10: 712-721.
- Carroccio A., Mansueto P., D’Alcamo A., Iacono G. Nonceliac wheat sensitivity as an allergic condition: personal experience and narrative review. Am J Gastroenterol 2013; 108: 1845-1852.
- Hollon J., Puppa E.L., Greenwald B. et al. Effect of gliadin on permeability of intestinal biopsy explants from celiac disease patients and patients with nonceliac gluten sensitivity. Nutrients 2015; 7: 1565-1576.
- Sapone A., Lammers K.M., Casolaro V. et al. Divergence of gut permeability and mucosal immune gene expression in two gluten-associated conditions: celiac disease and gluten sensitivity. BMC Med 2011; 9: 23.
- Portincasa P., Bonfrate L., de Bari O. et al. Irritable bowel syndrome and diet. Gastroenterol Rep (Oxf) 2017; 5: 11-19.
- Vazquez-Roque M.I., Camilleri M., Smyrk T. et al. A controlled trial of gluten-free diet in patients with irritable bowel syndrome-diarrhea: effects on bowel frequency and intestinal function. Gastroenterology 2013; 144: 903.e3-911.e3.
- Wu R.L., Vazquez-Roque M.I., Carlson P. et al. Gluten-induced symptoms in diarrhea-predominant irritable bowel syndrome are associated with increased myosin light chain kinase activity and claudin-15 expression. Lab Invest 2017; 97: 14-23.
- Fritscher-Ravens A., Schuppan D., Ellrichmann M. et al. Confocal endomicroscopy shows food-associated changes in the intestinal mucosa of patients with irritable bowel syndrome. Gastroenterology 2014; 147: 1012.e4-1020.e4.
- Schuppan D., Zevallos V. Wheat amylase trypsin inhibitors as nutritional activators of innate immunity. Dig Dis 2015; 33: 260-263.
- Reig-Otero Y., Manes J., Manyes L. Amylase-trypsin inhibitors in wheat and other cereals as potential activators of the effects of nonceliac gluten sensitivity. J Med Food 2018; 21: 207-214.
- Gomez L., Martin E, Hernandez D. et al. Members of the alpha-amylase inhibitors family from wheat endosperm are major allergens associated with baker’s asthma. FEBS Lett 1990; 261: 85-88.
- Junker Y., Zeissig S., Kim S.J. et al. Wheat amylase trypsin inhibitors drive intestinal inflammation via activation of toll-like receptor 4. J Exp Med 2012; 209: 2395-2408.
- de Punder K., Pruimboom L. The dietary intake of wheat and other cereal grains and their role in inflammation. Nutrients 2013; 5: 771-787.
- Murray K., Wilkinson-Smith V., Hoad C. et al. Differential effects of FODMAPs (fermentable oligo-, di-, mono-saccharides and polyols) on small and large intestinal contents in healthy subjects shown by MRI. Am J Gastroenterol 2014; 109: 110-119.
- Spiller R. How do FODMAPs work? J Gastroenterol Hepatol 2017; 32 Suppl 1: 36-39.
- Catassi C., Elli L., Bonaz B. et al. Diagnosis of non-celiac gluten sensitivity (NCGS): the Salerno Experts’ Criteria. Nutrients 2015; 7: 4966-4977.








