Для просмотра доступных исследований и сроков их выполнения
Выбранный город: Черкассы

Наследственный ангионевротический отек
15.05.2023
Наследственный ангионевротический отек (НАО) – редкое генетически обусловленное заболевание, характеризующееся повторными эпизодами невоспалительного отека кожи или слизистых без уртикарных высыпаний и зуда.
Синонимы заболевания:
- врожденный ангионевротический отек (HAE, HANE);
- дефицит С1-ингибитора комплемента;
- дефицит С1-ингибитора эстеразы;
- дефицит ингибитора C1-эстеразы (C1-INH, C1NH, C1-INH-HAE).
Что такое наследственный ангионевротический отек?
НАО впервые описан Уильямом Ослером в 1888 г. как семейная форма ангионевротического отека (АН). За шесть лет до этого в 1882 г. Генрих Квинке описал аллергический ангионевротический отек, и оба отека долгое время объединяли общим названием – отек Квинке. В 1963 г. было сделано открытие, что в основе наследственного рецидивирующего ангионевротического отека лежит дефицит ингибитора С1-эстеразы (Donaldson и Evans, 1963), в последствии был установлен аутосомно-доминантный тип наследования данного заболевания. Позже были открыты более редкие варианты, не связанные с дефектом С1-ингибитора, однако с аналогичными клиническими проявлениями.
НАО составляет около 2% от всех случаев ангиоотека, поэтому настороженность относительно этой разновидности является низкой, что приводит к значительным задержкам в диагностике, ухудшению качества жизни и высокому риску тяжелых осложнений при отеке в области гортани вплоть до летального исхода при отсутствии специфического лечения.
У больных с неустановленным диагнозом риск смерти из-за отека гортани может достигать 30–40%. Без лечения пациент с частыми приступами может пропустить до 100–150 рабочих дней в году. Своевременная диагностика позволяет определить правильную тактику лечения. Доступность терапии внушает надежду на улучшение качества жизни таких пациентов, снижение инвалидизации и летальных исходов.
Этиология, классификация и патогенез
На сегодняшний день известно две группы врожденного ангионевротического отека:
- Первая группа обусловлена дефектами С1-ингибитора (C1-INH-HAE) – как количественным (НАО I типа), так и качественным (НАО II типа);
- Вторая не связана с дефектами С1-ингибитора (nC1-INH-HAE) – ранее известная как НАО III типа.
НАО I типа возникает в результате сниженной концентрации ингибитора эстеразы компонента С1 комплемента в крови, этот вариант дефекта встречается в 90% случаев заболевания.
НАО II типа отвечает за > 10% и обусловлен функциональным дефектом ингибитора С1-эстеразы (снижение активности белка) при нормальной или повышенной его концентрации. Ген, ответственный за развитие как количественного, так и качественного дефектов С1-ингибитора эстеразы, расположен на длинном плече 11 хромосомы (11q12-q13.1) и называется SERPING1 (OMIM no. 606860; GenBank NM_000062.2). De novo мутации встречаются около 25% НАО I типа, поэтому не все пациенты имеют отягощенный семейный анамнез. Дефицит С1-ингибитора имеет аутосомно-доминантный тип наследования, то есть риск передачи заболевания потомству составляет 50% во время каждой беременности независимо от пола плода.
С1-ингибитор является ключевым регулятором системы комплемента, системы коагуляции крови и калликреин-кининовой системы. В период острой атаки ангионевротического отека происходит расщепление кининогенов, субстратов калликреина, возрастает концентрация брадикинина. Брадикинин – мощный сосудорасширяющий медиатор. Таким образом, в отличие от аллергического, медиатором отека при НАО является брадикинин, а гистамин и другие медиаторы тучных клеток не участвуют в его развитии. Также в отсутствие С1-ингибитора активация С1-эстеразы приводит к бесконтрольной активации классического пути с чрезмерным расщеплением С4 и С2 компонентов комплемента и образованием вазоактивного пептида С2b, эффект которого на посткапиллярные венулы проявляется развитием ограниченного отека.
Наследственный ангионевротический отек, не связанный с дефектом С1-ингибитора (nC1-INH-HAE), ранее классифицировавшийся как НАО III типа, является очень редким состоянием (менее 1%), вызываемым изменениями в генах фактора XII (FXII- HAE), плазминогена (PLG), ангиопоэтина 1 (ANGPT1), в кининогенном гене 1 (НАО-KNG1), в гене myoferlin (НАО-MYOF) и НАО в гене гепарансульфат 3-O-сульфотрансферазы 6 (НАО- HS3ST6).
Различные типы имеют общие черты патогенеза и клинической картины.
Клинические проявления
Отеки при НАО носят периодический характер, частота и тяжесть приступов имеют индивидуальную вариабельность.
В отличие от аллергического, отек развивается постепенно в течение 4-6 часов и сохраняется обычно в течение 24-72 часов. Приступы самолимитированы, продолжительностью 2–4 дня. Частота атак варьирует от еженедельной до одного или двух эпизодов в год и может изменяться в течение жизни пациента.
Первые признаки заболевания в 75-98% случаев появляются в детском и подростковом возрасте, но могут быть маловыраженными и нераспознанными, тяжесть симптомов усиливается в пубертатный период и во взрослом возрасте.
Триггерами чаще выступают:
- физические факторы;
- механическая травма или механическое давление (сидение на твердом, тесная обувь и т.п.);
- сильный болевой раздражитель;
- хирургическое вмешательство;
- стоматологические процедуры;
- интеркуррентное заболевание;
- эмоциональный стресс.
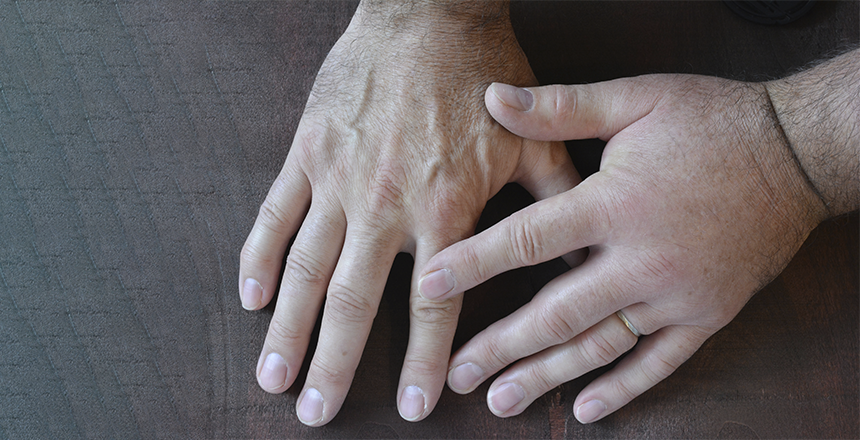
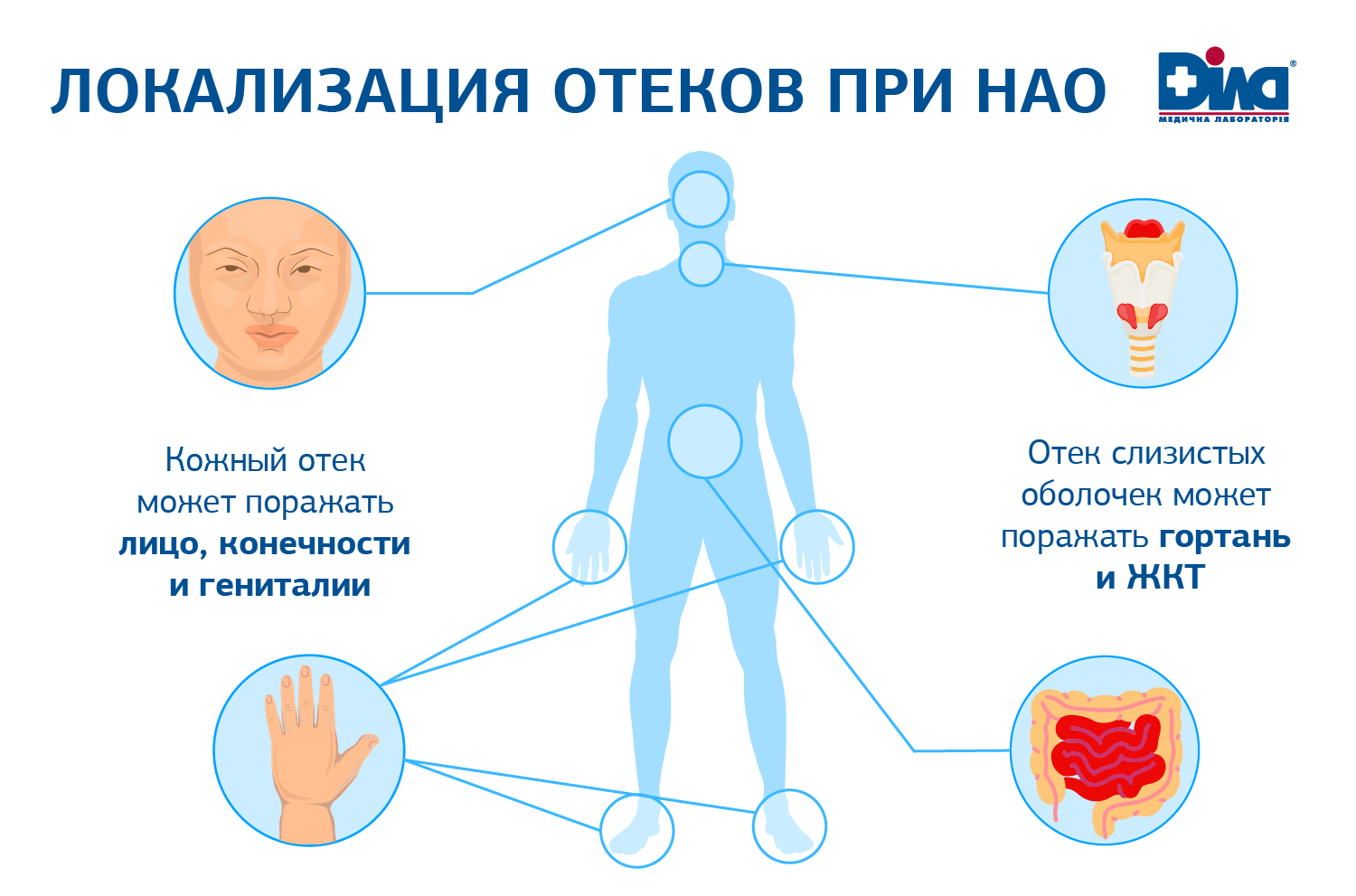
При отеках кожи наиболее частыми локализациями являются руки, ноги, веки, губы и гениталии, хотя вовлечен может быть любой участок кожи.

Гиперемия, локальное повышение температуры не характерно.
Хотя отеки кожи обычно не угрожают жизни, они нередко уродуют внешний вид, вызывают острую боль и приводят к снижению функции, например, конечности, во время приступа. Нередко приступы НАО охватывают несколько частей тела. Отек в области лица и шеи может распространиться на слизистую дыхательных путей.
Отек гортани встречается примерно у половины всех пациентов с дефицитом С1-ингибитора в течение жизни и может быть фатальным. Удаление зуба и оперативные вмешательства на челюстно-лицевой области – самые частые триггеры отека гортани. Отек горла и гортани приводит к затруднению глотания (дисфагия), осиплости голоса, затруднению разговора, может сопровождаться болью, затруднением дыхания, стридором и опасной для жизни асфиксией. Наличие даже одного отека гортани невыясненной природы показывает исключение НАО.
Симптомы, связанные с отеком слизистой пищеварительной системы включают тошноту, рвоту, острую боль в животе или даже признаки непроходимости кишечника. Отек пищеварительного тракта может проявляться сильной абдоминальной болью при полном отсутствии отеков на коже. Приблизительно каждый третий пациент с недиагностированным НАО испытывает ненужное хирургическое вмешательство во время абдоминальных приступов, так как по симптомам они напоминают состояние, требующее неотложной хирургической операции.
У некоторых больных накануне отека развиваются изменения кожи по типу кольцевидной эритемы. Эти изменения могут быть ошибочно приняты за крапивницу.
Около 50% пациентов отмечают все три варианта локализации отека в течение жизни (кожи, гортани, интестинальные).
Данные семейного анамнеза важны для диагностики заболевания, однако их отсутствие не исключает диагноза.
Диагностика НАО
Установление диагноза НАО I и II типа базируется на результатах сбора анамнеза и лабораторного обследования.
В основе диагностического алгоритма ДІЛА предлагает исследование Комплекс №237 "Диагностика наследственного ангионевротического отека (НАО)".
Комплекс (определение функции ингибитора C1-эстеразы, концентрации (уровня) белка C1-INH и C4 компонента комплемента в сыворотке/плазме) позволяет диагностировать заболевание, используя все три показателя в соответствии с международными рекомендациями (WAO/EAACI, 2017; The International/Canadian Hereditary Angioedema Guideline, 2019; US HAEA (Медицинская Advisory Board 2020 Guidelines for Management of Hereditary Angioedema).
При проведении трех тестов (функции ингибитора C1-эстеразы, концентрации (уровня) белка C1-INH и C4 компонента комплемента) диагностическая точность обнаружения НАО-1/2 выше по сравнению с использованием одного из них.
Для установления диагноза исследования системы комплемента проводят не менее 2 раз с интервалом более 1 месяца.
Особенности обследования на фоне лечения НАО: определение показателей системы комплемента неинформативно на фоне лечения концентратом С1-ингибитора. Обследование пациента проводят не ранее чем через 1 неделю после введения концентрата С1-ингибитора или плазмы и через 3 недели после окончания лечения андрогенами.
При нормальных показателях С4, концентрации и активности С1-ингибитора в помощь для подтверждения диагноза придет лишь молекулярно-генетическое обследование с секвенированием генов, ответственных за развитие наследственного ангионевротического отека, не связанного с дефектом С1-ингибитора (FXII-HANG, PL , KNG1, MYOF, HS3ST6), однако на сегодняшний день открыты не все дефекты в генах, которые могут быть вовлечены в патогенез наследственного ангионевротического отека.
Лечение
Для лечения НАО используются следующие группы препаратов: на основе С1-ингибитора (концентрат, полученный из плазмы, рекомбинантный), ингибитор калликреина, антагонист брадикининового рецептора. Тактика ведения пациентов с АН включает лечение острых атак и меры по профилактике приступов (долговременная и краткосрочная профилактика).
В прошлом для покупки острого эпизода также применялись антифибринолитики (такие как аминокапроновая и транексамова кислота) или андрогены (даназол). На сегодняшний день эти препараты не рекомендованы, поскольку они оказывают минимальный эффект при остром приступе.
С рекомендованных международным протоколом препаратов для украинских пациентов доступен концентрат С1-ингибитора в пределах государственной закупки для пациентов с редкими болезнями. Концентрат С1-ингибтора может использоваться как для покупки острых приступов, так и для коротко- и длительной профилактики. Препарат приводит к повышению уровня C1-INH в плазме крови и помогает регулировать все каскадные системы, участвующие в продукции брадикинина во время атак. Для получения терапии в пределах государственной закупки пациенты с НАО или подозрением на НАО должны быть направлены к иммунологу (взрослому или детскому).